����1 ����(Introduction)
��ѧ�������������Է�ˮ�о��ж������������オ����л���Ⱦ�������Ч������.���и���������(Advanced Oxidation Technologies, AOTs)������Ч�Ļ�ѧ��������֮һ, ��ʵ����ˮ�Ĵ����з�������Ҫ����.��AOTs��, ��Ӧ��ѭ���е�����;��, ͨ�������γɸ��Ե����ɻ�, �硤 OH��SO4-��.��Щ���ɻ��Ļ�ѧ���Ժܸ�,����������Щ����, ��ѧ�Һ���ʦ��һֱ�����ڿ�����Ӧ�ø��ָĽ���Fenton������������������.���귢չ�����Ļ�����������ɻ�(SO4-��)�����������������л���Ⱦ���ȥ��Ч����, ����Ӧ��Χ��.�ü����Ե��������λ��߹���������Ϊ������, ʹ�ù��ɽ���Co2+��Ag+��Cu2+��Fe2+��������䡢O3���ȵ�����Ϊ����, �������Ե���������ɻ�SO4-�����ڰ������ݼ���ɱ����������ڷ��ڸ����ż��Ⱦ�ϡ��������ʵȶ����л���Ⱦ��ĸ�Чȥ��.��ʹ�÷Ǿ�������������ڴ����ķ�����ظ�����, �Ҳ��ٹ��������Ч������������������һ��ľ������ϵ.����, Pu���о���Fe/S�ӻ��Ļ���̿������Ч���������ν�����Ⱥ��ڱ������������;�Ա��о���ʹ�õ���̼���ܡ����̼CMK-8����ԭ������ʯīϩ��������θ�Ч����ȥ�������Ⱦ����Ⱦ���Ч��, ������Щ�ǽ���������Ч���ȴ�ͳ�Ľ���������(Fe3O4��CuO��Co3O4��MnO2)Ч������.��ǰ�ø�����������ҪΧ�����ʹ������Ʊ��ͻ����, ����Ⱦ��ȥ��������̽����չ��.�ڴ�ͳ�����ʹ���ʽ�Ļ�����, �ǽ������ʼ���Ȼ�л�����Ϊ���, �����˹㷺�Ĺ�ע���о�.������������ɱ�����, �����Ѻ��Ҹ�Ч, ��Դ�㷺, �����ڸ�����������ԭλ���е�Ӧ��.
�������͵�̼���������̿��̼���ܡ�̼��ά������ϩ������ʯīϩ������صĽṹ�ͻ�ѧ����, �ڻ�����Ⱦ����������չʾ�����õ�����.����, ��櫶Դ���̼���ܼ��临�ϲ�����ˮ���ؽ�����Ⱦ���������˽�Ϊϵͳ���о�;ʹ�û���̿��Ϊ���������ߴ���Ҳ�����˹㷺�Ĺ�ע(�����2006).��������������ʯīϩ�Ļ���Ӧ���о�ҲԽ��Խ��, ���磺�о�������ʯīϩ���ϲ��Ϲ�������л����Ч��;ʹ�ø�������ʯīϩ��Ϊ������, ���ڻ�����Ⱦ���ȥ���ͺ�����Ⱦ��ĸ�������Ҳ����α���.����ʯīϩ����ĵ��Ӵ�������, �ḻ�Ĺ��ܻ��źͱ��漰��Ե��ȱ�ݽṹʹ���ڹ������ѧ�������е�Ӧ��ǰ������.��ͨ��������л�ѧ����, ��ǽ���Ԫ�ص����ס���IJ���, �ͽ����������γɸ��ϲ��ϸ����ؿ��˸ò��ϵ�Ӧ��.Wang�ȵ��о�����������������ʯīϩ��, ���BPA���������������ӵ�����ʯī��1.75��, ���������ν���BPA�ķ�Ӧ���ʳ�������ͨ����ʯīϩ��700��, ����Ч���������.ʹ�õ���������Fe3O4���ߴ��������ϲ�����Ϊ�����ڸ����������е�Ӧ���о�Ҳ�õ��˽�ȫ����о�.��������Fe3O4�������д�ıȱ����, ����λ���, �Ҵ�������ʹ������Ϊ������ʱ��, ���ڴӷǾ�����ϵ�з������, ���ڲ������ظ�����.�����о������Ʊ����Ե���ʯīϩ��Ϊ���, ּ�ڽ�����ʯīϩ�Ķ������ܺʹ�������Fe3O4����������, ����, ������̼���ϵ��л�����, ��������ЭͬЧӦ, �ٽ������, ��߽���Ч��.
�������о��ӵ�ǰˮ��Ⱦ�������ٵ���ս����, ���ø���������ȥ��ˮ���л���Ⱦ���Ч����������, ������ʯīϩ���ص�̼ԭ�ӽṹ, ����ĵ��Ӵ������������ڻ�ѧ���Ե���������, ͬʱ������ϴ���, �Ʊ����Ե���ʯīϩ, ��������жλ����.Ȼ���Ը����ͽ���̼�����ϲ���Ϊ����, ��������Ϊ������, ���γɸ��Ե����ɻ�, ������Ⱦˮ�����Ǽ����Ľ���.ϵͳ�о��˽����е���ҪӰ������, ����Ӧ����ѧ, ���ɻ���������Լ��Ǽ����Ľ���;��.�÷�������Ч, ����Ϊ�л���ˮ, ������Ⱦ�Ϸ�ˮ�Ĵ����ṩһ�ּ���Ч��������Ⱦ�ļ�������֧��.
����2 �����뷽��(Materials and methods)
��������ʯīϩ(GO)Ϊ����ĩ״, �������ݺ���ʯīϩ�Ƽ�����˾, ��ѧ�Լ��Ǽ�����������ء����������������������ء��������ơ����ᡢ��ˮ���״����Ҵ���KI��DMPO��Ϊ�Լ���, ���ڹ�ҩ���Ż�ѧ�Լ�����˾.ʵ��ȫ���ó���ˮ.���õ���Ҫ�����豸����������-�ɼ��ֹ��ȼ�(�Ϻ��ǵ������������˾)������Ʒ��ǿ��(VSM)(�Ͼ��ϴ�����)��JSM-6700Fɨ���������(�ձ�����JEOL)������˳�Ź���EPR (�ձ�����JES FA 200)��X����������(�¹���³D8)��BET�ȱ����������(����Quantachrome, USA)�����л�̼������(TOC-V CPH�ձ�����).
����2.1 ���Ե���ʯīϩ���Ʊ��ͱ���
��������0.5 g����ʯīϩ(GO)������ɢ��150 mLˮ��.Ȼ�����ˮ�ȷ����������������������������ε�GO����.�������Ϊ����GOˮ��Һ�зֱ����һ����������������������, ʹ�������������ʵ����ı�Ϊ2:3, ��85 ���ˮԡ�����н����ܽ�, Ȼ��е�����ٶȵ���500~600 r��min-1, ����4 mol��L-1��ˮ, ������ϵpHΪ9~11, ��������45 min, �õ�����GO(M-GO).��M-GO���Է�����ϴ, �����ĥ��, �ٽ��е�������.������Ϊ��Դ�ͻ�ԭ��, ���Ʊ���M-GO��ɢ��ˮ��, ����һ����������, ʹ������GO��������Ϊ30:1, ����ܽ��Ϻ�, ����Һ��ϵ����180 ���ˮ�ȷ�Ӧ���з�Ӧ18 h, �õ����Ե���ʯīϩM-N-G.���ڵ���ʯīϩ(N-G)���Ʊ�, ֱ����GO����M-GOΪԭ��, ����Ϊ��Դ�ͻ�ԭ��, ��180 ���ˮ�ȷ�Ӧ���з�Ӧ18 h�õ�.����SEM��BET��XRD��VSM�����ֶζ�����Ե���ʯīϩ�ı�����ò�ͽṹ����ѧ���ʽ��з���.
����2.2 ���Ե���ʯīϩ������������ϵ�Ĺ����Ͳ����Ż�
������50 mL 10 mg��L-1���Ǽ�����Һ�зֱ����10 mg��M-N-G��0.4 mmol��L-1�Ĺ��������Һ, ˮԡҡ���ܹ��һ��ʱ��, �����併���Ǽ�����Ч��.���в���UV-VIS (����ɼ��ֹ��ȼ�)��665 nm�²ⶨ�Ǽ���Ũ��.�Ǽ����Ľ�������Ct/C0��ʾ, ����CtΪtʱ����Һ��ϵ���Ǽ�����Ũ��, C0Ϊ�Ǽ����ij�ʼŨ��.
����������Һ��ϵpH��2~8��Χ��, �Խ���Ч����Ӱ��.�ֱ�����������ƺ��������pH.���촦��ʱ����¶ȶԽ���Ч����Ӱ��.�ֱ���15~32 ����, ��ͬ��ʱ���(5~120 min��ȡ��), �ⶨ����Ч��, ������н����ѧ������ѧ����.����Թ�����ص�������M-N-G��Ͷ����Ҳ������̽��.�����Ǽ���������TOC�IJⶨҲ����50 mL, 10 mg��L-1�Ǽ���Ϊ��Һ��, ����10 mg��L-1 M-N-G��0.4 mmol��L-1�Ĺ������, ÿ��һ��ʱ��ⶨ��ϵ�е�TOC, TOC��ȥ���ʲ���(TOC0-TOCt)/TOC0��100%��ʽ������, ����TOC0��10 mg��L-1�Ǽ��������л�̼����, TOCt��tʱ�̲�õ����л�̼����.ʹ�ú��M-N-G, ����0.1 mol��L-1��������ϴ, Ȼ�����ó���ˮ��ϴ����ظ�����.
����3 ʵ���������(Results and discussion) 3.1 ���ϵı�������
�����Ʊ���M-N-G������Ϊ��ɫ�ķ�ĩ״, �����ɢ��ˮ��, ���ⲿ������������, ���Ժܺõķ���.Ϊ�˽�һ���˽���ϵ��۽ṹ������, ���Ȳ��ó�����ɨ��羵��GO��N-G��M-N-G������ɨ��.�����ͼ 1��ʾ.

����ͼ 1 GO(a)��N-G(b)M-N-G(c)��SEMͼ��
������ͼ 1���Կ���, GOΪƬ��״�ṹ, �Ƕ��GO������һ��Ľ��, ���治ƽ��, ��ȴ����5~8 nm֮��, �������������κ͵���������, ���ϵ��ž�������, �����д���Fe3O4��������, ����Fe3O4������500 nm��1 ��m�����ȷֲ�, Fe3O4�������ϴ��ҷֲ��ȽϿ�, ��������Ϊ�ڲ��ӵ���ˮ�ȷ�Ӧ������, ����������ʯīϩ�ϵ�Fe3O4��һ���ۺ϶����µ�.��SEMͼ��Ļ�����, ����XRD, ��һ���������ϳɷ�.�����ͼ 2��ʾ.���ϳ�����Fe3O4�ĵ��������.˵��Fe3O4���ܺõ����ε�GO����.����Ʒ��ǿ�Ʒ����Ĵ���ǿ��Ϊ42.5 emu��g-1.�����۵Ľ��Ҳ֤ʵ�����Ͼ������õĴ���, ���ⲿ�ų���������, ����Ч������, ��ͼ 3��ʾ.

����ͼ 2 M-N-G��XRDͼ��

����ͼ 3 M-N-G��ɢ��ˮ�е�״̬(a)�����ⲿ�������õķ���Ч��ͼ(b)
������ͬһ����Ʒ�ֱ�����˴��Է�������ķ����������, �����Һ����ⶨ�Ǽ���Ũ��, �������ߵIJ���������0.1%, ˵�����Է�������dz���Ч.�ں����IJ���������, �ⶨ��Ʒǰ�ķ�������������ⲿ�ų���������ɵ�, �������IJ��������ķ���.
��������BET�ȱ�����Ϳ������ǶԺϳɵIJ��Ͻ����˷���.���о�������GO�ıȱ����ԼΪ175 m2��g-1(�Լ���˾�ṩ), ���δ���Fe3O4��, ���ϵıȱ�������͵�117.32 m2��g-1, ������������, ���ϵıȱ������һ������, Ϊ94.35 m2��g-1.��Ҳ������һ������˵���������κͲ��������Ƿ�����GO�ı����, ͨ������Fe3O4�Ͳ�������, ��ʹGO�ıȱ��������.GO�����������κ͵�������, �����������.����ֱ�Ϊ5.221 nm(GO)��3.8605 nm(M-GO)��3.745 nm(M-N-G).����IUPAC����(Sing, 1989), �������ͼ�������ж�, M-GO�ĵ��������Ѹ�������H4�ͺ�IV������, ��M-N-G�����Ѹ������Ǿ���H3�ͺ�IV������.���GO�����Ľṹ�������ͺ����Ϳ����ж�, �����Դ��Ҫ��Ƭ״GO�ѻ��γɵ������.���������κ�, ���Ľ���, ����ܵ�ԭ����, ����������ʻ���뵽GO�ļз�ṹ, ʹ�����С.

����ͼ 4 M-GO (a)��M-N-G(b)��N2���Ѹ�����BJH���ֲ�ͼ
����3.2 ��ͬ���ϵ�������Ч���Ա�
����Ϊ��ѡ����ѵIJ�����Ϊ����, �ֱ�����˵���ʯīϩ(N-G, 5 mg)����������ʯīϩ(M-GO, 10 mg)�����Ե���ʯīϩ(M-N-G, 10 mg)��Fe3O4(10 mg)��Ϊ�������ʹ���, �Լ���������������(0.4 mmol��L-1)�����Ǽ�����Ч��.��ͼ 5���Կ���, N-G������Ч�����, ����Ҫ����Ϊ�ò�����ʯīϩ�ı������.M-N-G�Ĵ��������, ������M-GO�Ĵ�Ч��, ������Ϊ��������, ���뵪ԭ�ӽ��뵽GO�Ľṹ��, һ���������GO�ĵ�����, ��һ����������GO��ȱ�ݽṹ, �����ڵ��ӵĴ���(������, 2012;����˫��, 2017).������Fe3O4�������ʹ�Ч�������߱�����, ����ֻ�������������, ����Fe3O4��, ��������������, ˵��Fe3O4�߱�һ���Ĵ�Ч��, �ý����֮ǰ�Խ�Ӣ�о�����һ��(2010).���ϱȽ�, �ں�����ʵ���в���M-N-G��Ϊ����.

����ͼ 5 ��ͬ���ϵ�������Ч���Ա�
����3.3 pH�Դ���Ӱ��
��������������������ˮ������ʱ��, ��Һ��ϵ��pH�Խ���Ч��Ӱ������.��ΪpH����Ӱ������Ļ���, �����������������Լ���������Ⱦ��Ĵ���״̬.�ڱ��о���, �����о���ϵpH�Խ���Ч�ʵ�Ӱ��.�����ͼ 6��ʾ.
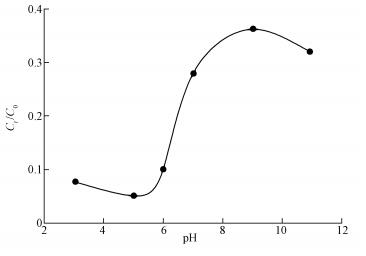
����ͼ 6 pHֵ���Ǽ�������Ч�ʵ�Ӱ��
������ͼ�п��Կ���, ��pH=3~11��Χ��, �����ʶ�����60%, ���ڴ�ͳ�ķҶ���������.��Ҳ�ʹ����ױ������.����pH�Ľ�����(90%~95%)���Ժ������Ժͼ�������(62%~72%), ��������������pHֵ�Ľ����ʲ��첻��.����ܵ�ԭ���ǣ��������������ڻ����Fe2+���ͷ�, ���ͷŵ�Fe2+����������γ���������ɻ�, �����Ǽ����Ľ���.����pH������, Fe2+���ͷż���, ��������ɻ���������, ���Ҽ��������������ǻ����ɻ����γ�, �������������ɻ�(t1/2=30 ~40 ��s), �ǻ����ɻ�(t1/2 < 1 ��s)����������(Oh et al., 2016), ����Ч���õ����ɻ���������.���о���, �Ǽ���������Һ��pH�ӽ�6, ��ϵ�ڸ���Һ������, ���Ա���һ���ϸߵĽ���Ч��, ���, ����������, û�ж���ϵ��pHֵ���е���.
����3.4 �����¶ȶԽ����Ӱ��
�����������ʳ������������⼼���е�һ����Ҫ����, ֱ�ӹ�ϵ���ü���������Ч�ʺͳɱ�.�����¶ȶԴ����ⷴӦ�����ʳ���Ӱ������.�ڱ��о���, ̽��15��21��32 ����, ���ϵĴ�����.���Dz��Ͼ��нϴ�ıȱ����, ���Ǽ�����һ������������.���Ƚ�M-N-G���뵽�Ǽ�����Һ��, ��������1 h��, �ټ��������ؽ��д������, ÿ��һ��ʱ��ȡ���ⶨŨ��.�����ͼ 7��ʾ.

����ͼ 7 �¶ȶ��Ǽ���ȥ���ʵ�Ӱ��
������ͼ 7���Կ���, M-N-G���Ǽ�����һ��������Ч��, ��15~32 ���������, ��������ȥ����ϵ��15%~25%���Ǽ���.�����������Ժ�, �Ǽ�����ȥ�����������, 2 h�Ժ�, ������ԼΪ93%.�����¶ȵ�����, �����ٶ�����, ��2 h�Ĵ���Ӧ������, ǰ1 h��Ӧ�Ͽ�, ����Ϊ�Ǵ���Ӧ�Ŀ��ٷ�Ӧ��, ��2 h����Ϊ�����ٷ�Ӧ��.����αһ������ѧ���̽������, ����15��21��32 ��ʱ��Ӧ�Ľ������ʳ���k�ֱ�Ϊ0.0227��0.0271��0.0488 min-1.���ݰ�������˹��ʽ(lnk=lnA-Ea/RT, lnk~1/T��ͼ, ��б�ʿɵñ��ۻ��Ea)����Ļ��Ϊ33.7 kJ��mol-1.Wen��(2014)ʹ���������������ν���������ȱ��Ļ��Ϊ31.79 kJ��mol-1, Kang��(2016)ʹ�õ����ӻ�ԭ����ʯīϩ��������ν��⿹���صĻ��Ϊ38.6 kJ��mol-1.
����3.5 ����������س�ʼŨ�ȶԽ���Ч�ʵ�Ӱ��
���������˼��벻ͬŨ�ȴ���, ���Ǽ�������Ч�ʵ�Ӱ��.��ͼ 8a���Կ���, 0.5 mmol��L-1������ؿ���ȥ����ϵ��Լ40%���Ǽ���.������Ϊ���������Ϊһ��������, ���������ԭ��λE0=1.96 V, ��˿�����һ���̶��Ͻ����Ǽ���.�����ļ���, �����������Ⱦ���ȥ����.������ϵ�л����������80 mg��L-1���ӵ�280 mg��L-1, ����Ч�ʴ�70%���ӵ���95%.����200 ~280 mg��L-1�������, ����Ч�ʼ����ӽ�, ��Щ˵�����ܻ����������ϵ����Ч��Ӱ���ش�, �������ӵ�һ��Ũ�ȵ�ʱ��, ����Ӱ�������ʧ.��ԭ����, ��ϵ�й�����ص���������, ��M-N-G���ӵ�200 mg��L-1ʱ, ���ܹ������0.5 mmo��L-1����Ҫ����, ���, �����ӻ������Ӱ�첻��.

����ͼ 8 M-N-G����(a)�������������(b)�Խ���Ч�ʵ�Ӱ��
�����ڷ���M-N-G�������Խ���Ч�ʵ�Ӱ���, �������������������������Ӱ��.��ͼ 8b���Կ���, M-N-G�߱�һ������������, ����ȥ����ԼΪ20%.��ΪM-N-G�ıȱ����Ϊ94.35 m2��g-1(BET�������), ����ͨ����������ȥ����Һ�е��Ǽ���, ����ʯīϩ����Ħм�Ҳ�ɺ��Ǽ������ý�������.��������ص�Ũ�ȴ�0.02 mmol��L-1���ӵ�0.5 mmol��L-1ʱ, ����Ч�ʴ�50%���ӵ���95%, ���Ҵ�0.2 mmol��L-1��0.5 mmol��L-1, ����Ч�ʶ���90%����, �仯����.��Щ˵��, ������ؾ������, �γ����ɻ�, �����Ǽ����������������.�����������Ũ������һ���̶ȵ�ʱ��, �����Ӵ�����, Ч��С, ������Ϊ��ϵ�е�M-N-G������һ����, ֻ����Ч�һ�����Ĺ������, �������ŷ�Ӧ�Ľ���, �м���������, �λ��IJ���ʧ�������, Ҳ�ᵼ�»���Ļ��Խ���.���������о������������ο�����Ϊ���������������ɻ���Ӧ(Anipsitakis et al., 2003), ����ͼ 8b��ʾ�Ľ����, ��û����������.�����ԭ���ǣ���������y��Ӧ���ٶȱ����������Ǽ������ٶ�С;����M-N-G�߱�һ���������Ǽ�������Һ, �����γ���������ɻ����ȷֲ���M-N-G����Χ, ������������ɻ����Ǽ������������, ����ڱ���ϵ��, �϶�Ĺ�����ز�û�ж���ϵ������������.
����ͼ 8�Ż�����ϵ������������������, �Եõ���ѵĽ���Ч��.ͨ���Ż�������ϵ������Ũ��Ϊ200 mg��L-1, �������Ũ��Ϊ0.4 ~0.5 mmol��L-1, ��10 mg��L-1���Ǽ�����ȥ���ʸߴ�95%, ���ǿ̶����?ͼ 9Ϊ��ϵ�ڲ�ͬ�����µĿ���.���Կ���, ���ԼΪ50%, ��˵���Ǽ����ڽ����Ĺ�����, �������ֿ�ΪCO2��H2O��, ���������л����ʵ�����.

����ͼ 9 �Ǽ���ȥ�������е����л�̼TOC��ȥ����
����3.6 ���ɻ��γ����༰�����������
���������о�������������������α����, �ܹ�������������ɻ�, Ȼ����������ɻ��ֿ��Ժ�H2O��OH-��Ӧ, �����ǻ����ɻ�.ͨ����ϵͨ����������ɻ����ǻ����ɻ�������ȥ����Ⱦ��(Fang et al., 2013; 2017).����M-N-G�������ص�ʱ��, ��ϵ�����ɻ�������������?ͨ��EPR�������������ɻ��y��ʵ�����һ̽����.����0.1 mol��L-1 DMPO��Ϊ�����, ������ϵpHΪ6, �������µIJⶨ�����ͼ 10��ʾ.��������ɻ����ǻ����ɻ����źŶ��м�.����•�����ǻ����ɻ������ط�(1:2:2:1), ��������������ɻ������ط�(1:1:1:1:1:1), ˵����ϵ���������ɻ���ͬ��������.�״����Ҵ�ͨ����������ѧ������������ǻ����ɻ�����������ɻ�������.��������ɻ���״����Ҵ���Ӧ�����ʳ����ֱ�Ϊ3.2��106��1.6��107 L��mol-1��s-1, ���ǻ����ɻ���״����Ҵ���Ӧ�����ʳ����ֱ�Ϊ��9.7��108��1.9��109 L��mol-1��s-1(Oh et al., 2016), �����˼״����Ҵ��ļ���Խ���Ч�ʵ�Ӱ��(�ֱ�ʹ��10��100���������Ũ��).�����ͼ 11��ʾ�����ִ��Խ���Ч��Ӱ��С, ������KI��(1����2���������Ũ��), ����Ч����������.�״����Ҵ���Ϊ���õĴ����, �ڱ�ʵ����, û��������, ��KI�ĝy��Ч������.���Ƶ�����Ҳ������(Xu et al., 2012; Wang et al., 2015).����ܵ�ԭ������Ϊ��ˮ�ԵĴ������ʷ�ɢ��ˮ��, ���������γ���M-N-G��������ɻ���Ӧ.

����ͼ 10 ����Ӧϵͳ��EPRͼ��
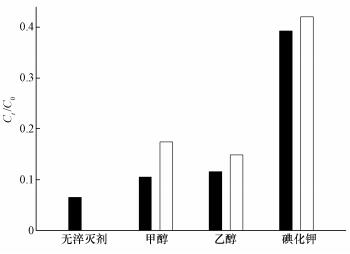
����ͼ 11 ��ͬ������µĽ���Ч��
���������о�����������Ǽ�����ȥ�������ɻ���������Ϊ��, ͬʱҲ�в��������ڹ�����ص�ֱ������, �Լ�M-N-G������ȥ��.��M-N-G����������ͨ��Fe2+��������Fe3+�ṩ����, ��GO��Ϊ��������, �ﵽ��Ч��������ز�����������ɻ�.
����3.7 �����ظ�������
����M-N-G��Ϊ����, ���ظ����ô����Բ��ϵ��ۺ���������������Ҫ.ʹ�ú�Ļ��, ���ⲿ�ų���������, ����ϵ�з������, Ȼ�����0.1 mol��L-1 H2SO4��ϴ��, ���ó���ˮ��ϴ, �ظ�����4�εĽ����ͼ 12��ʾ.
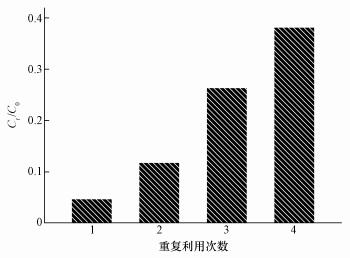
����ͼ 12 ����ظ�����Ч��ͼ
������ͼ�п��Կ���, ��4��ʹ��ʱ, �併������Ȼ�ɴ�60%, �߱��Ϻõ��ظ�����Ч��.���´������Ա���ԭ���������ʹ����, ����λ�㱻�����ڴ���������Ǽ������м����ռ��, ���������, ���ⷴ��ʹ�õĹ�����, ����λ�����ʧ��.����μ���ˮ���̳����ϻ�http://www.dowater.com������ؼ����ĵ���
����4 ����(Conclusions)
�������о���̽����ʹ��M-N-G��Ϊ���, ��������ز�����������ɻ�����ˮ���Ǽ�����Ч��.����M-N-G���Ʊ�������, ��������, BET�ȱ����Ϊ94.35 m2��g-1, ����СΪ3.745 nm.��ϵ��pH 2~6ʱ, �ܹ�����ȥ����ϵ��90%���Ǽ���, �����Ժͼ���������, ����Ч�ʵ���70%.ͨ�������ѧ������ѧ������������15~32 ����, ��ϵ�Ľ������ʳ�����0.042 min-1��0.109 min-1֮��, ��Ӧ�Ļ��Ϊ33.7 kJ��mol-1.ͨ�����������������Ż��о�������M-N-G�߱���������ȥ���Ǽ���������, �������Ҳ����ͨ�������������������ⲿ���Ǽ���.�������Ե���GO��Ũ��Ϊ200 mg��L-1, �������Ũ��Ϊ0.2~0.5 mmol��L-1ʱ, �ܹ�����ȥ��95%Ũ��Ϊ10 mg��L-1���Ǽ���, ��TOC��ȥ���ʿɴ�50%.EPR����������ɻ��y��ʵ������������ϵ����Ҫ��������������ɻ�Ϊ��.�ظ�ʵ�����������ô������Է�������4�κ�, ����Ч����Ȼ�ɴ�60%.���о���չʾ�ļ�����������Ч, ��������, Ϊ��Ⱦˮ����л���Ⱦ������, ������Ⱦ�Ϸ�ˮ�����ṩ�������ݺͼ������.


