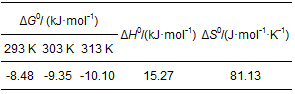1 引言 (Introduction)
铀矿冶生产中产生了大量的低浓度含铀废水, 如不妥善处理直接排放, 对生态环境和人体健康将构成潜在的严重威胁, 有效处理含铀废水显得尤为重要 .含铀废水的主要处理方法有化学沉淀法、生物修复法、膜分离法和吸附法等, 其中吸附法因其高效廉价、操作简单、无二次污染且便于铀回收利用的优点而备受关注, 成为铀矿冶环境治理的研究热点.
氧化石墨烯 (GO) 是石墨氧化的产物, 表面富含羧基、羟基等含氧基团, 且比表面积较大, 对重金属离子有很好的吸附效果研究发现氧化石墨烯对U (Ⅵ) 的最大吸附量达111.7 mg・g-1, 明显高于其它铀酰离子吸附剂.但由于氧化石墨烯具有亲水性, 吸附后难以从水中分离, 在实际应用中可将GO与其它吸附材料复合, 既可以提高GO的吸附能力, 又使其便于分离回收.壳聚糖 (CS) 是甲壳素脱乙酰化的产物, 其分子结构中存在大量的氨基和羟基, 具有吸附性能好、易再生和价廉等优点.但CS能溶于酸性溶液, 这极大地限制了它的应用, 因此有必要对CS进行交联改性, 使直链的CS分子形成网状结构, 从而提高其在酸性溶液中的稳定性.有研究表明, 将壳聚糖接枝到氧化石墨烯上得到的CS/GO复合材料热稳定性高、机械性能好, 对Au3+, Pd2+等有毒重金属具有良好的吸附效果.但有关CS/GO吸附热力学、动力学及机理等方面的研究还不够深入, 且将其应用于低浓度含铀废水处理的报道相对较少.本研究利用Hummers法合成氧化石墨烯并与壳聚糖进行混合, 经戊二醛交联改性后制备出吸附位点多, 不溶于酸, 且可过滤分离的CS/GO复合材料.探讨了CS/GO对U (Ⅵ) 的吸附特性, 通过SEM-EDS、FTIR、XRD等表征手段研究其吸附机理, 以期为CS/GO处理含铀废水提供理论依据.
2 材料与方法 (Materials and methods) 2.1 主要试剂与仪器
主要试剂:天然鳞片石墨 (325目), 青岛金日来石墨有限公司;壳聚糖 (脱乙酰度大于90%), 国药集团化学试剂有限公司;硝酸钠、高锰酸钾、氢氧化钠、盐酸 (37%)、戊二醛等其他试剂均为市售分析纯, 模拟含铀废水采用U3O8(分析纯) 根据GBW04201配制而成.
主要仪器:台式恒温振荡器 (IS-RDD3, 美国精骐有限公司);pHS-3C型精密酸度计 (上海雷磁仪器厂);扫描电子显微镜 (JSM-7500F, 日本电子);X射线能谱仪 (Energy 350, 英国牛津仪器有限公司);傅里叶变换红外光谱仪 (NICOLET6700, 美国Themo Fisher公司);X射线衍射仪 (D8 Advance, 德国布鲁克AXS公司);紫外可见分光光度计 (T6, 北京普析通用公司).
2.2 壳聚糖/氧化石墨烯的制备
采用改进的Hummers法制备氧化石墨.称取一定量研磨好的氧化石墨加到25 mL体积分数为1%的乙酸水溶液中, 室温下超声45 min, 形成均匀悬浊液.不断搅拌的同时逐步加入0.5 g壳聚糖粉末, 超声1 h, 使壳聚糖与氧化石墨烯混合均匀, 再加入1.5 mL 50%的戊二醛作为交联剂, 继续搅拌1 h.静置12 h, 将分散良好的悬浊液用0.1 mol・L-1的NaOH溶液浸泡, 使复合物变成凝胶状, 将产物过滤并依次用50%的乙醇溶液和超纯水洗涤、烘干、研磨、过筛 (0.15 mm), 密封干燥备用.
2.3 吸附试验
取50 mL一定浓度 (2~100 mg・L-1) 的铀溶液置于150 mL锥形瓶中, 用0.1 mol・L-1的HCl和NaOH溶液调节pH值 (2~8), 加入适量 (0.05~0.40 g・L-1) 吸附剂, 恒温振荡 (20~40 ℃, 150 r・min-1) 一定时间 (5~420 min) 后过滤, 用紫外分光光度计在578 nm处测定滤液U (Ⅵ) 浓度, 试验重复3次, 取平均值.分别按式 (1) 和式 (2) 计算CS/GO的吸附量q(mg・g-1) 和U (Ⅵ) 的吸附率η:
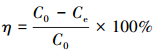
式中:C0、Ce分别为吸附前后溶液中U (Ⅵ) 的浓度 (mg・L-1);V为溶液体积 (L);m为吸附剂的投加量 (g).
2.4 解吸试验
将0.4 g・L-1的CS/GO投加到pH=5, U (Ⅵ) 初始浓度为150 mg・L-1的溶液中, 30 ℃恒温振荡5 h后过滤, 测定滤液中U (Ⅵ) 的剩余浓度.再将吸附后的CS/GO放入100 mL 0.1 mol・L-1的HCl溶液中, 振荡解吸120 min, 过滤并测定滤液U (Ⅵ) 浓度.将解吸后的CS/GO用去离子水反复洗涤若干次, 烘干后再在相同条件下进行吸附-解吸试验, 循环利用4次.U (Ⅵ) 的解吸率按照式 (3) 计算:
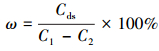
式中:C1为U (Ⅵ) 的初始浓度 (mg・L-1);C2为吸附后溶液中的U (Ⅵ) 浓度 (mg・L-1);Cds为解吸液中U (Ⅵ) 的浓度 (mg・L-1).吸附和解吸过程中溶液的体积相同.
3 结果与讨论 (Results and discussion) 3.1 GO含量对CS/GO吸附U (Ⅵ) 的影响
在pH值为5, CS/GO投加量为0.2 g・L-1, U (Ⅵ) 初始浓度为10 mg・L-1, 温度为30 ℃, 吸附时间为5 h的条件下, CS/GO中GO的质量分数 (5%~70%) 对吸附效果的影响如图 1所示.
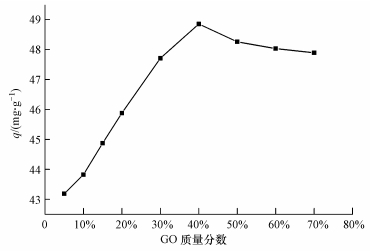
图 1 GO含量对CS/GO吸附U (Ⅵ) 的影响
由图 1可见, CS/GO对U (Ⅵ) 的吸附量随GO含量的提高先快速增加后逐渐减小.这是因为GO的加入增大了CS/GO的比表面积, 提供更多的含氧基团 (羟基、羧基等), 使得CS/GO的吸附能力增强.当GO质量分数为40%时, 吸附量达到最大值.但继续提高GO含量, 吸附量反而略有降低, 可能是GO上的羧基和CS的氨基发生酰胺化反应, 形成―NHCO―键, 从而降低了羧基和氨基对铀酰离子的螯合能力 (He et al., 2011).在后续试验中, 均采用GO质量分数为40%的CS/GO复合材料进行吸附试验.
3.2 pH值对CS/GO吸附U (Ⅵ) 的影响
在U (Ⅵ) 初始浓度为10 mg・L-1, 吸附剂投加量为0.2 g・L-1, 温度为30 ℃, 吸附时间为5 h的条件下, pH值对GO、CS、CS/GO吸附效果的影响如图 2所示.
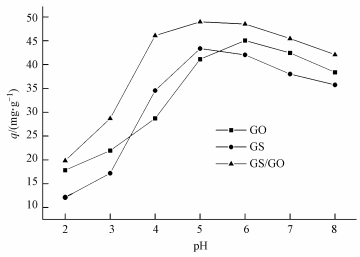
图 2 pH值对U (Ⅵ) 吸附的影响
从图 2可以看出, CS/GO对U (Ⅵ) 的吸附量明显高于CS和GO, pH值对3种材料吸附效果的影响均较大.当pH<5时, 随着pH值的升高, 吸附量逐渐增大.因为pH值较低时, 溶液中大量的H+与UO22+竞争吸附剂上的结合位点, 同时CS和GO表面的活性基团易被质子化而带正电, 增强了CS/GO对UO22+的静电斥力, 故吸附量较低 (郑伟娜等, 2011).随着pH值的升高, CS和GO上游离活性基团 (如―NH2、―COOH等) 的含量逐渐增加, 其络合能力也随之提高.当pH为5~6时, 3种材料的吸附量达到最大值.pH>6时, 吸附量反而减小, 这是由于溶液中UO22+易发生水解, 形成UO2(OH)3-、UO2(OH)42-等络合负离子, 与CS/GO表面活性基团产生静电斥力作用, 阻碍吸附反应的进行;同时溶液中CO32-、HCO3-离子增多, 易与UO22+形成难以被吸附的碳酸铀酰络合物 (Zou et al., 2012).因此CS/GO去除U (Ⅵ) 的最佳pH值选为5.
3.3 投加量对CS/GO吸附U (Ⅵ) 的影响
在pH值为5, U (Ⅵ) 初始浓度为10 mg・L-1, 温度为30 ℃, 吸附时间为5 h的条件下, CS/GO投加量 (0.05~0.40 g・L-1) 对吸附效果的影响如图 3所示.
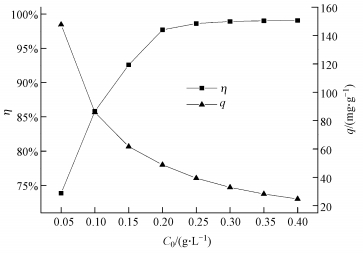
图 3 CS/GO投加量对U (Ⅵ) 吸附的影响
由图 3可知, 随着CS/GO投加量的增加, U (Ⅵ) 的吸附率η逐渐提高, 而吸附量q却逐渐降低.这可能是用量的增加使得CS/GO上活性位点的数目增多, 铀酰离子与活性位点结合概率增大, 故U (Ⅵ) 的吸附率随之上升.当CS/GO投加量较低时, 其表面的氨基、羟基等结合位点能被充分利用, 随着投加量增加, 吸附剂相互碰撞团聚导致活性基团利用率下降, 从而导致吸附量减小 (陈月芳等, 2013).当CS/GO投加量为0.2 g・L-1时, U (Ⅵ) 的吸附率达97.70%, 继续增加投加量, 吸附率增加很小.考虑吸附效果且使吸附剂能被充分利用, 试验中CS/GO的最佳投加量定为0.2 g・L-1.
3.4 反应时间对CS/GO吸附U (Ⅵ) 的影响及动力学分析
在pH值为5, CS/GO投加量为0.2 g・L-1, 温度为30 ℃的条件下, 反应时间 (5~420 min) 对初始浓度分别为5、10、15 mg・L-1含铀废水吸附效果的影响如图 4所示.
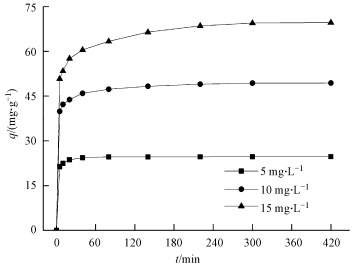
图 4 反应时间对U (Ⅵ) 吸附的影响
从图 4可以看出, 在吸附的前5 min, CS/GO对U (Ⅵ) 的吸附量急剧增加, 此后5~300 min吸附量上升减缓, 300 min后吸附趋于平衡.这是由于吸附初期CS/GO上有大量的结合位点, 溶液中UO22+的浓度较高, 使得吸附驱动力较大;而随着吸附的进行, 有效活性位点被不断占据, 吸附驱动力减弱, 导致吸附速率变慢.当吸附时间达到300 min后, CS/GO上的活性位点被基本占据, 吸附达到平衡.因此, 确定最佳吸附时间为5 h.
为了探讨扩散速率与速率控制步骤对CS/GO吸附过程的影响, 分别采用准一级、准二级动力学模型和颗粒内扩散模型对试验数据进行拟合, 结果如表 1所示.由表 1可知, 准二级动力学模型中3个浓度的可决系数R2均大于0.999, 且理论平衡吸附量qe, cal接近实际值qe, exp, 说明准二级动力学模型更适合描述CS/GO对U (Ⅵ) 的吸附过程, 由此表明该吸附为化学吸附, U (Ⅵ) 主要通过化学键合作用结合在CS/GO表面 (季雪琴等, 2016).另外, 颗粒内扩散模型的拟合直线不经过原点, 表明颗粒内扩散不是CS/GO吸附U (Ⅵ) 的速率控制步骤.
表 1 吸附动力学参数
3.5 吸附等温线及热力学分析
在pH值为5, CS/GO投加量为0.15 g・L-1, 温度分别为20、30、40 ℃, 吸附时间为5 h, U (Ⅵ) 的初始浓度为2、5、10、15、20、30、40、50、70、100 mg・L-1的条件下, CS/GO对U (Ⅵ) 的吸附等温线如图 5所示.
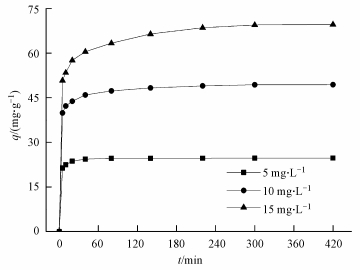
图 5 CS/GO对U (Ⅵ) 的吸附等温线
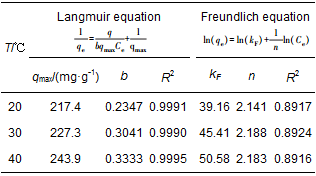
从图 5可以看出, 随着平衡浓度的升高, CS/GO对U (Ⅵ) 的吸附量也逐渐增加, 且吸附效果与温度正相关.采用Langmuir和Freundlich等温吸附方程对吸附过程进行拟合, 结果如表 2所示.由表 2可知, Langmuir等温吸附方程的可决系数R2均大于0.999, 而Freundlich等温吸附方程拟合度较低, 说明CS/GO对U (Ⅵ) 的吸附是单分子层吸附;Freundlich方程中的参数n均大于2, 表明吸附较易 (李凯斌等, 2014);在Langmuir等温吸附方程中, 初始浓度为10 mg・L-1的铀溶液在3个温度下的分离因子RL(表 2 U (Ⅵ) 的等温吸附方程和拟合参数
利用焓变ΔH0、熵变ΔS0和吉布斯自由能变ΔG0来分析温度对CS/GO吸附过程的影响, 计算公式如下:
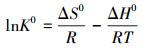
式中:ΔH0(kJ・mol-1) 和ΔS0(J・mol-1・K-1) 可视为不随温度改变的常数, 不同温度的吸附平衡常数K0可按以下方法 (Al-othman et al., 2011) 计算:在不同温度下分别作lnKd(Kd=qe/Ce) 对Ce的线性图 (如图 6), 当Ce趋近于0时即得到该温度的lnK0.

图 6 lnKd与Ce的关系线
再根据方程 (5), 通过lnK0对1/T做图 (图 7), 由拟合直线的斜率和截距分别计算出ΔH0和ΔS0, 计算结果见表 3.
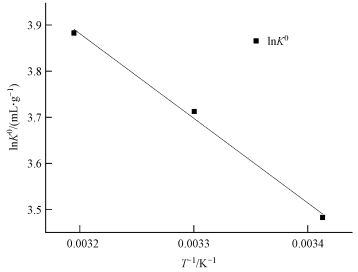
图 7 lnK0与1/T的关系线
表 3 CS/GO吸附铀的热力学参数
由表 3可知, CS/GO对铀的吸附过程中吉布斯自由能变ΔG0均为负值, 表明吸附反应是自发进行的 (Subbaiah et al., 2011);温度越高, ΔG0越小, 说明升温将促进吸附, 这与试验结论相符;焓变ΔH0>0, 说明吸附是吸热反应;熵变ΔS0>0, 表明吸附过程中固液交界面的混乱程度增大, CS/GO对铀酰离子具有一定的亲和作用 (王哲等, 2015).
3.6 CS/GO的吸附解吸试验
通过解吸试验可以了解吸附剂的循环次数, 以判定其能否重复利用.由前述试验可知, 在强酸条件下, CS/GO对U (Ⅵ) 的吸附率较低, 因此可通过H+与UO22+之间的离子交换作用来对CS/GO进行洗脱.选用0.1 mol・L-1的HCl溶液作解吸剂, 4次吸附/解吸循环下CS/GO对U (Ⅵ) 的吸附率/解吸率如图 8所示.
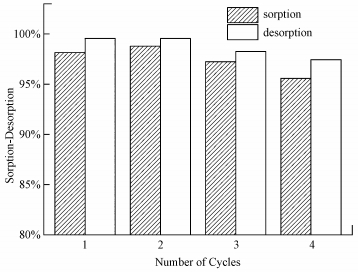
图 8 U (Ⅵ) 的吸附与解吸
由图 8可知, 初次解吸率高达99.55%, 解吸一次后吸附率反而略有增加, 这可能是经HCl处理后, CS/GO表面增加了更多的吸附位点.经4次吸附解吸试验后, CS/GO的吸附率仍高达95%以上, 表明CS/GO具有良好的再生与循环利用性.
3.7 扫描电镜及EDS能谱分析
图 9为GO、CS以及CS/GO吸附U (Ⅵ) 前后的扫描电镜图.从图中可以看出, GO呈单层片状结构, 表面光滑, 局部地方出现弯曲和褶皱;CS表面致密均匀, 没有明显的凸起和孔隙;而CS/GO表面粗糙, 凹凸不平, CS与GO结合较为紧密, 材料具有更多的吸附位点和更大的比表面积, 有利于其对铀酰离子的吸附.对比图 9c、d可知, 吸附U (Ⅵ) 后CS/GO的形态结构发生明显变化, 表面变得较平整, 孔隙减少, 这可能是铀酰离子与CS/GO中的有机官能团相互键合的结果 (聂小琴等, 2013).

图 9 GO (a)、CS (b) 和CS/GO吸附U (Ⅵ) 前 (c)、后 (d) 的扫描电子显微镜图
CS/GO吸附U (Ⅵ) 前后的EDS分析结果如图 10所示.从图中可以看出, 吸附前后都有C、N、O、Au存在, 其中Au是照射前的喷金处理导致的, 而壳聚糖和氧化石墨烯中含有大量的C、N、O是图中C、N、O元素含量较高的原因.吸附后材料中出现很强的铀峰, 表明CS/GO对U (Ⅵ) 具有一定的吸附能力.

图 10 CS/GO吸附U (Ⅵ) 前 (a)、后 (b) 的X射线能谱分析图
3.8 傅里叶红外光谱分析
图 11为GO、CS以及CS/GO吸附U (Ⅵ) 前后的红外光谱图, 由谱线a可知, GO在3428 cm-1处有一个宽强峰, 为―OH的的伸缩振动峰;在1732、1615、1395和1105 cm-1处分别是C=O和C=C的伸缩振动峰、叔羟基的特征峰以及环氧基C―O―C的伸缩振动峰 (Yang et al., 2010).CS红外光谱图中3485 cm-1处是―NH2和O―H的伸缩振动重叠峰, 1662 cm-1处则属于“酰胺Ⅰ带”上C=O的伸缩振动峰 (Wang et al., 2009).
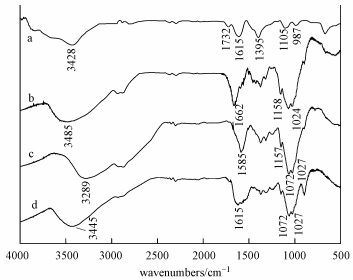
图 11 GO (a)、CS (b)、CS/GO (c)、CS/GO-U (Ⅵ)(d) 的红外光谱图
CS/GO的IR吸收曲线中, 在3289 cm-1处的峰为仲酰胺―NH和―OH相互重叠形成的伸缩振动峰, 该峰相对于CS在3485m-1处的峰出现偏移, 可能是CS上的―NH2与GO的―COOH反应生成酰胺引起的.1585 cm-1处的峰是壳聚糖“酰胺Ⅱ带”烷基伯酰胺―NH2的弯曲振动峰, 1072 cm-1处是GO上环氧基C―O―C和CS上脂肪伯胺C―NH2的重叠峰, 1157 cm-1和1027 cm-1处的峰则分别来自壳聚糖C6位叔醇基团C6―OH和C3位C3―OH的吸收峰, 上述结果表明CS/GO成功合成.
比较CS/GO吸附前后的FTIR结果可知, CS/GO吸附U (Ⅵ) 后有部分峰位置偏移或者强度发生变化.其中, 3289 cm-1处的峰消失, 在3445 cm-1处出现强度减弱的谱峰, 这可能是由于―OH与U (Ⅵ) 通过氢键发生了配位络合, 而酰胺基N―H未参与反应.1585 cm-1处的峰偏移到了1615 cm-1处, 表明烷基伯酰胺―NH2参与了铀的螯合.此外, 1072 cm-1和1027 cm-1处的峰强明显减弱, 说明脂肪伯胺C―NH2和C3―OH基团也参与了U (Ⅵ) 的吸附.以上结果表明, 在CS/GO对U (Ⅵ) 的吸附过程中, 羟基和氨基为主要吸附位点.
3.9 X射线衍射分析
在对CS/GO表面形貌和官能团分析的基础上, 利用X-射线衍射对其晶体结构进行表征, 如图 12所示.从图中可以看出, GO在2θ=10.6°处出现了一个反应GO (100) 晶面的特征峰, 说明石墨已经被充分氧化成GO (吴敏杰, 2011).CS在2θ=20.7°的峰对应于壳聚糖的无定形结构.而复合材料CS/GO在2θ为10.6°和20.7°附近的特征衍射峰强度均明显减弱, 这可能是GO和CS之间的相互作用影响了CS分子链在晶格中的排列, 并导致GO不能相互堆积形成有序结构.
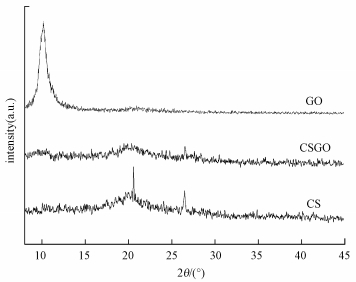
图 12 GO、CS和CS/GO的XRD图
4 结论 (Conclusions)
1) 利用Hummers法合成氧化石墨烯 (GO) 并与壳聚糖 (CS) 进行混合, 经戊二醛交联改性后, 制备得到CS/GO复合材料.
2) CS/GO对U (Ⅵ) 具有良好的吸附性能.当GO质量分数为40%, pH值为5时吸附效果最好, 吸附平衡时间为5 h, 30 ℃时理论饱和吸附量为227.3 mg・g-1.Langmuir等温吸附方程和准二级动力学模型 (R2>0.999) 能较好地拟合CS/GO对U (Ⅵ) 的吸附过程.CS/GO吸附U (Ⅵ) 是自发的吸热反应.吸附解吸试验表明CS/GO具有良好的再生与循环利用性.具体参见污水宝商城资料或http://www.dowater.com更多相关技术文档。
3) SEM-EDS、FTIR和XRD分析表明, CS/GO吸附U (Ⅵ) 的过程中, 参与反应的基团主要有羟基和氨基;吸附U (Ⅵ) 后CS/GO表面变得平整光滑, 孔隙明显减少.