近年来,世界范围内的地下水污染日趋严重,其中硝酸盐氮的污染不断加剧。因硝酸盐氮在水和土壤中的高溶解性和迁移性以及生活污水和工业废水的直接排放、含氮化肥的大量使用、污水灌溉以及畜禽粪便和其他含氮固废的淋滤下渗,使得地下水中硝酸盐氮浓度不断增加,2006―2012年,河北省地下水中硝酸盐氮平均含量增加了46.42%。硝酸盐氮可在人体中转化,直接、间接地危害人体健康,因此研究地下水中硝酸盐氮的脱除具有重要意义。目前所采用的离子交换、电渗析、反渗透等处理技术,因运行费用高、操作复杂、需后处理,而受到限制;单质铁化学还原法脱氮技术,因需调节水质pH反应条件难以控制,且伴有副产物氨氮生成,而无法推广应用;生物反硝化脱氮因地下水中缺乏碳源,而无法满足脱氮要求;利用投加液态碳源进行反硝化脱氮,因投加量难控会导致出水有机物风险;利用人工合成聚合物固态碳源进行反硝化脱氮,因成本高、对温度和pH要求高、需额外投加微量元素克服其化学成分单一性而难以实施;利用天然生物质进行反硝化脱氮,会出现生物可利用性低、反硝化效率低、亚硝酸盐氮积累等问题;利用Fe0与棉花组合,虽可有效降低水中硝酸盐氮浓度,但无法克服Fe0的钝化影响。目前,水体脱氮研究多集中在为生物反硝化提供更佳的碳源或将生物与化学多种方法组合等。
本研究利用自制微电解化学催化颗粒与天然生物质制成耦合生物载体,将化学还原与生物反硝化相结合高效脱氮,通过研究耦合生物载体脱氮的可行性和稳定性,以及反应器中微生物群落结构,探究其脱氮机制,为地下水硝态氮脱除提供理论依据和技术指导。
1 实验材料和方法
1.1 实验材料
自制微电解化学催化固体颗粒以铁、碳、多元催化剂为主要原料烧制而成[8,16],如图1(a)所示,其直径10~20 mm,比重1 200 kg・m−3,比表面积32.017 m2・g−1,孔隙率46%,物理强度≥600 kg・cm−2。粗糙多孔,利于传质及微生物附着,并且可发生原电池反应还原硝酸盐氮。天然生物质丝瓜络含有79.5%左右的纤维素、13.6%左右的木质素,在水中可分解产生多糖或单糖等小分子糖类,为微生物提供一定的营养。将丝瓜络经水洗风干后切割成50~100 mm,并于40 ℃烘干,与微电解化学催化固体颗粒组合制成如图1(b)所示的耦合生物载体。
图1 自制微电解化学催化固体颗粒与天然生物质耦合生物载体
1.2 实验装置
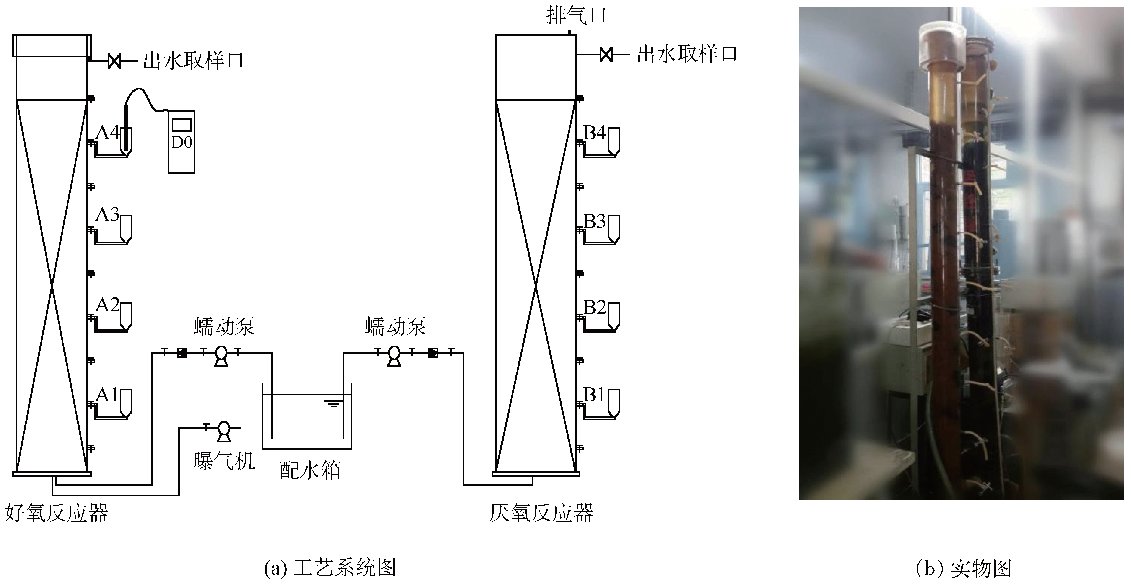
实验装置见图2。反应器采用有机玻璃材料制成,高度为2 000 mm,好氧反应器直径100 mm,底部安装有曝气头;厌氧反应器直径110 mm;耦合生物载体填充深度(1 630±10) mm;反应器每隔400 mm设1个取样口,共设8个。反应器均采用逆流下进上出的进水方式连续运行,通过进水计量泵来控制流速。
图2 反应装置
1.3 实验用水
实验水质参照华北地区中度污染的地下水水质,使用KNO3、NH4Cl和NaNO2进行配制,如表1所示。本研究所用化学药品均为分析纯。
表1 实验用水水质指标(均值±标准差)
1.4 水质指标分析及方法
各水质指标分析方法均参考《水和废水监测分析方法》中的方法。硝酸盐氮、亚硝酸盐氮、氨氮分别采用紫外分光光度法、N-(1-萘基)乙二胺分光光度法和纳氏试剂分光光度法,紫外-可见分光光度计为UV 2102C(UNICO company; USA);pH采用梅特勒-托利多实验室pH计进行测定;DO采用YSI便携式溶解氧仪进行测定。微生物群落分析,采用文献中的方法进行。
2 结果与讨论
2.1 反应器的启动
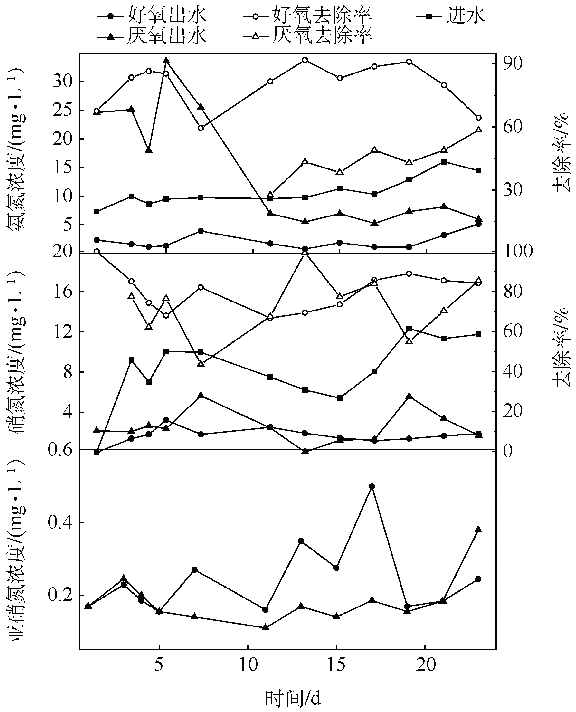
实验初期采用接种污泥的方式对反应器进行微生物挂膜培养,控制进水NO3−-N浓度(8.53±2.39) mg・L−1,NH4+-N浓度(10.35±1.96) mg・L−1,pH=6.89±0.80;水力停留时间(HRT)为20 h;好氧反应器溶解氧(DO)浓度为3.0 mg・L−1,厌氧反应器DO<0.1 mg・L−1。连续运行出水水质指标变化如图3所示。
反应器运行初期,厌氧反应器出水氨氮浓度高于进水且有60%左右的硝酸盐氮得到去除,表明初期硝酸盐氮的还原主要是化学催化固体原电池反应的结果,并伴有氨氮的生成。随挂膜培养时间的延长,硝酸盐氮的去除率有所增加,且未出现亚硝酸盐氮的积累,出水氨氮的浓度也明显降低,由25.32 mg・L−1降到7.00 mg・L−1以下,说明厌氧反应器内硝酸盐氮的还原由化学作用逐渐转为以微生物反硝化作用为主。天然生物质分解的小分子物质为微生物挂膜生长、生物反硝化提供了有效碳源,缩短了反应器的启动时间。好氧、厌氧反应器整体启动较为迅速,在15 d左右硝酸盐氮去除率分别达到87.5%和77.4%,表明挂膜成功,并在20 d逐步提升进水硝酸盐氮浓度以适应模拟地下水的水质。
图3 反应器启动期氮素的浓度变化
2.2 反应器的稳定运行
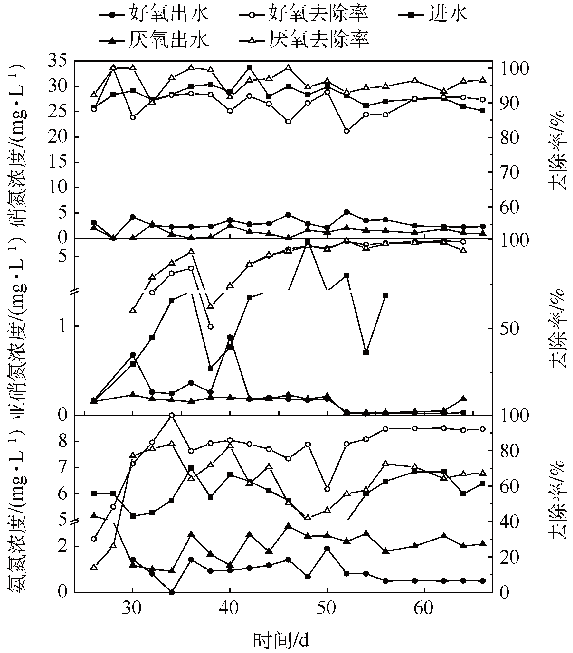
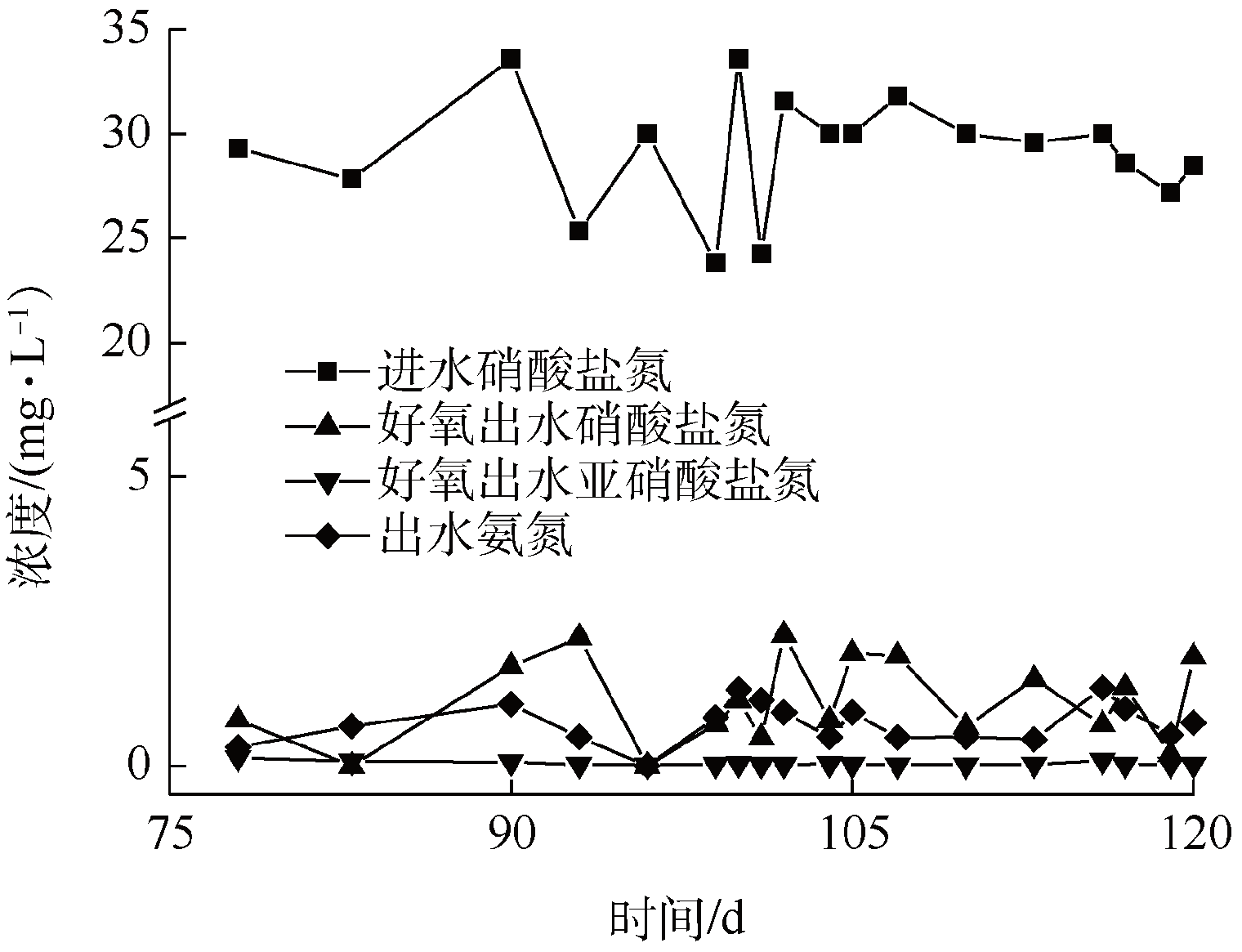
反应器挂膜培养成熟后稳定运行25~66 d,处理水质NO3−-N浓度为(29.54±1.97) mg・L−1,NH4+-N浓度(5.79±1.50) mg・L−1,pH=7.71±0.34,HRT=20 h,好氧反应器DO=3.0 mg・L−1,厌氧反应器DO<0.1 mg・L−1,水质变化见图4。由图4可知,好氧反应器的硝酸盐氮平均去除率为91.24%,平均出水浓度为2.539 mg・L−1;厌氧反应器的硝酸盐氮平均去除率为96.32%,平均出水浓度为1.036 mg・L−1。2个反应器都表现出较高的硝酸盐氮去除效率。分析原因主要是自制微电解化学催化固体颗粒与天然生物质耦合生物载体,将化学催化还原与生物自养、异养反硝化进行耦合的结果,充分利用自制微电解化学催化固体颗粒的原电池反应还原硝酸盐氮,同时为生物体系中自养反硝化菌提供所需的电子;利用天然生物质丝瓜络为异养反硝化菌提供必要的生长繁殖所需的有限有机物,实现联合高效脱氮。在整个反应体系中,细菌可以利用氢化酶加速催化固体颗粒的铁腐蚀,同时铁元素为微生物生长繁殖及酶辅基提供必要的微量元素,原电池反应过程中所产生的铁离子可提高生物脱氢酶等酶系的活性]。原电池反应、自养脱氮、异养脱氮三者协同作用的脱氮效果明显优于单一过程。此外厌氧反应器的pH(7.55~8.18)与好氧反应器的pH(8.25~8.57)都有利于硝酸盐氮的还原,为反硝化细菌提供更多的电子供给。CHENG等研究发现增加缓释碳源可以促进脱氮效率尤其是反硝化脱氮。
图4 反应器处理模拟地下水中氮素的浓度变化
主要反应原理见式(1)、(2):
NO3−+5H(电子供体)→1/2N2+2H2O+OH−(1)
6NO3−+C(有机磷)→3N2+6CO2+2H2O+6OH−(2)
反应器运行的50~66 d,2个反应器出水亚硝酸盐氮浓度均低于0.05 mg・L−1,达到了世界卫生组织对饮用水中0.91 mg・L−1的要求。此外,氨氮在好氧反应器中平均去除率为92.63%,平均出水浓度低于0.5 mg・L−1,达到了饮用水中氨氮0.5 mg・L−1的浓度要求,表明在好氧条件下硝化细菌活性高,能充分利用氨氮,并解决了化学原电池反应生成氨氮影响出水水质的问题,对模拟受污染地下水中低浓度氨氮有较好的去除效果;而在厌氧反应器中的平均去除率为68.32%,明显低于好氧反应器,分析原因是厌氧反应器内缺乏硝化作用功能菌,仅靠微生物同化作用去除氨氮的效率相对较低,但有研究发现厌氧环境下部分微生物也具有氨氧化能力,也有报道称发现异养硝化菌在完全厌氧条件下可发生硝化作用。具体联系污水宝或参见http://www.dowater.com更多相关技术文档。
2.3 反应器运行的影响因素
2.3.1 HRT的影响
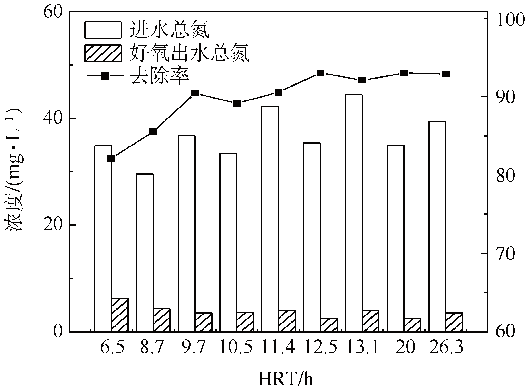
HRT是影响固态碳源反硝化的一个重要因素,HRT越长越利于水解酶分解产生可利用碳源;但是HRT过长,能耗高、不经济。因此,在2.2节中所述反应器稳定运行的条件下对HRT进行优化,好氧反应器选定9个水平HRT进行实验,分别为6、8、9、10、11、12、13、20和26 h;厌氧反应器的HRT分别为9、10、11、12、13、14、14.5、15和16 h。结果见图5和图6。
图5 不同HRT下好氧反应器中总氮的去除率
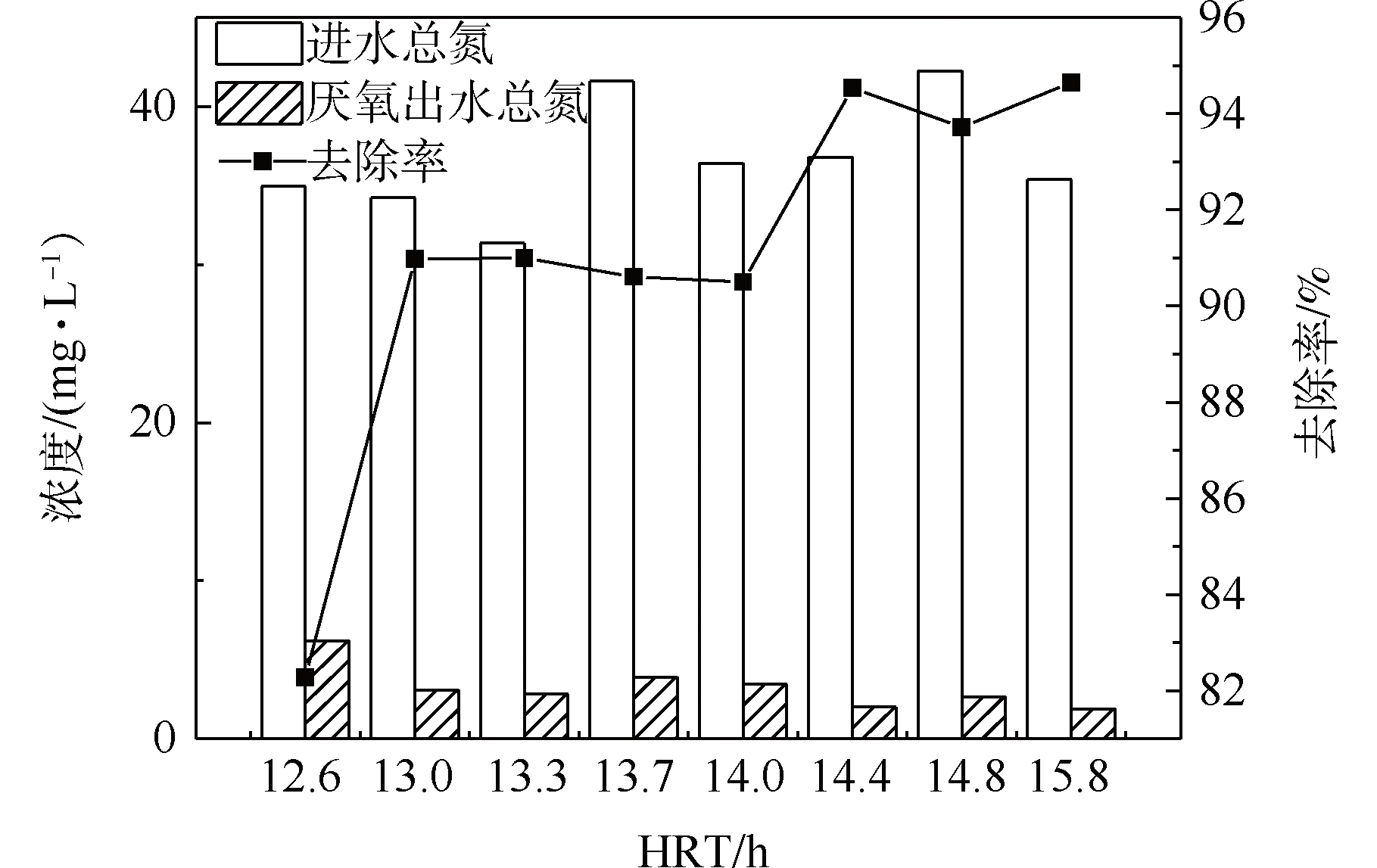
图6 不同HRT下厌氧反应器中总氮的去除率
由图5和图6可知,反应器硝酸盐氮的去除率随HRT的延长而增大并逐渐趋于稳定。说明随着HRT的延长,水中的氮素物质能够与反应体系中的各种微生物间充分地传质、接触、反应,且有机质充分水解提供充足的电子供体,此时HRT不再是反硝化的限制因素,继续延长HRT,对反硝化作用提高不明显。为使出水硝酸盐氮浓度达到《地下水质量标准》(GB/T 14848-2017)的Ⅱ类及以上,好氧反应器适宜的HRT为12 h;厌氧反应器为14 h。
2.3.2 DO对好氧反应器的影响
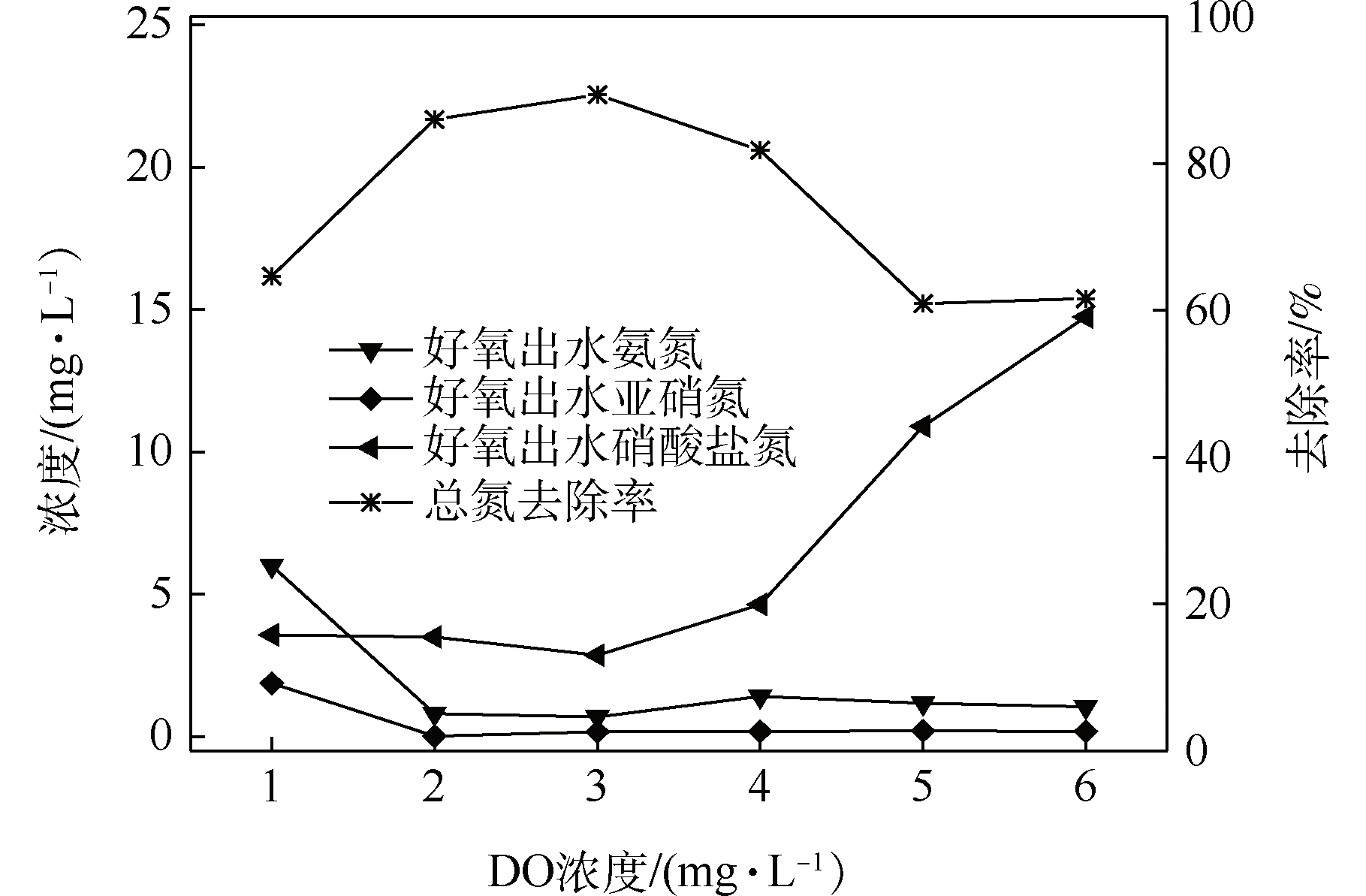
在2.2节中所述反应器稳定运行的条件下及2.3.1中最佳的HRT工况下,控制好氧反应器DO分别为(1.0±0.3)、(2.0±0.3)、(3.0±0.3)、(4.0±0.3)、(5.0±0.3)和(6.0±0.3) mg・L−1。结果见图7。由图7可知,DO<2 mg・L−1或DO>4 mg・L−1都会使好氧反应器的总氮去除率降低。DO浓度高时相应的曝气强度大,会导致水中的剪切力增大,使生物膜的脱落速度大于生物膜的生长速度;过大的曝气强度还会使水流的紊动加剧,紊动的水流会将载体上的生物膜冲刷下来,导致微生物的总量减少,还会影响出水水质。在氧气存在的条件下,反硝化细菌优先选择氧而不是硝酸盐氮作为电子受体,只有分子氧被耗尽,脱氮微生物才能开始利用硝酸盐氮;并且体系中有较强的还原能力的铁极易被氧化而降低其还原活性。DO浓度偏低时,导致硝化细菌的呼吸作用受抑制,因而影响其对氨氮的去除效果,进而降低了总氮的去除效率。为保证整个工艺的高效脱氮,硝化作用、反硝化作用都能够较好的发挥各自功能,DO应控制在2.0~3.0 mg・L−1。该浓度范围适合于浅层含氧的地下水修复。
图7 不同DO浓度下好氧反应器出水中各氮素变化及总氮去除率
2.4 厌氧反应器与好氧反应器串联运行
好氧反应器反硝化速率略低,厌氧反应器去除氨氮有限,为克服好氧反应器和厌氧反应器单独运行的不足,将厌氧反应器与好氧反应器串联,进水水质见表1,HRT=12 h,好氧反应器DO=2.0 mg・L−1,厌氧反应器DO<0.1 mg・L−1,室温22~25 ℃下稳定运行43 d。实验结果见图8。由图8可知,最终出水硝酸盐氮的平均浓度为1.231 mg・L−1,达到《地下水质量标准》(GB/T 14848-2017)的Ⅰ类标准要求,且没有亚硝酸盐氮和氨氮的积累。表明串联运行方式能在更短的HRT及较少的曝气量下实现更高的总氮去除率,出水总氮浓度(2.090 mg・L−1)低于单独运行时的好氧反应器(总氮浓度3.063 mg・L−1)和厌氧反应器(总氮浓度3.348 mg・L−1)。因此,利用厌氧反应器中反硝化作用去除硝酸盐氮,好氧反应器中的硝化作用去除氨氮,有利于反应器发挥各自优势,实现更高效率的脱氮效果。
图8 串联运行氮素的浓度变化
2.5 反应器内耦合生物载体中微生物分布及耦合机理
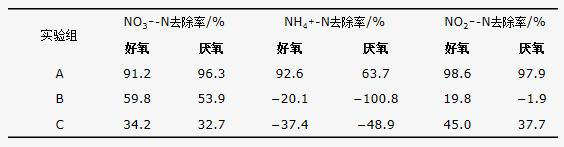
为进一步验证反应器中高效脱氮的耦合作用,从反应器中取出部分载体均分为A、B、C 3组,其中A组不做处理,为耦合生物载体;B组将微电解化学催化载体取出,为单独的生物质及其内部微生物;C组相反,将生物质取出,为单独的微电解化学催化载体及其内部微生物。将A、B、C 3组分别模拟好氧反应器和厌氧反应器的最佳运行条件及实验水质条件(见表1),结果见表2。
表2 验证耦合作用的烧杯实验
由表2可知,分离后的B、C对硝酸盐氮的去除率明显低于耦合载体A,且有氨氮、亚硝酸盐氮积累现象,表明在生物膜与化学载体耦合的作用下有良好的脱氮效果,原电池反应产生的微电场可以刺激增加微生物酶活性,同时微生物对化学催化载体有一定的表面更新作用,相互促进;B对硝酸盐氮的去除效率约为C的2倍,表明耦合体系中异养反硝化作用占主导,约为反硝化作用的2/3,形成以异养反硝化为主、自养反硝化及化学反应为辅的脱氮体系。
如图9所示,占优势的菌如Sulfuritalea、Thiobacillus、Ferritrophicum、Denitratisoma等都具有反硝化功能,与报道相一致。WANG等的研究发现固态有机物与ZVI组合有协同作用,王苏艳[33]也发现Fe2+和碳源有协同作用促进反硝化。此外铁是生物氧化酶系统中细胞色素的重要部分,且Fe2+和Fe3+的氧化还原反应中电子传递可以促进生化反应速率。由于生物质分解、发酵产酸(HCO3−和CO2)可中和反硝化过程产生的碱度及微电解化学催化固体原电池反应产生的氢氧根,反应器出水pH在保持在7.5~8.6,适宜微生物生长繁殖,利于反硝化过程稳定顺利进行,且自呈缓冲体系,无需外加缓冲剂。在2个反应器内实现化学与生物相耦合的反硝化过程,此外好氧反应器中还实现了同步硝化反硝化,对模拟受污染地下水的脱氮有突出效果。
图9 反应器中8个样品在属水平的相对丰度
3 结论
1)自制微电解化学催化固体颗粒与天然生物质丝瓜络制成耦合生物载体将化学反应与生物膜耦合,在实验室反应器中实现了地下水模拟水质硝酸盐氮的高效脱除,并使其达到了《地下水源质量标准》(GB/T 14848-2017)的Ⅰ类标准,且无亚硝酸盐氮和氨氮积累。
2)好氧、厌氧反应器的最佳水力停留时间分别为12 h和14 h;溶解氧偏高、偏低都限制好氧反应器的脱氮效果,在2.0~3.0mg・L−1达到最佳;将厌氧反应器与好氧反应器串联,出水总氮浓度最低为2.090 mg・L−1,效果最好。
3)硝酸盐氮的脱除是自制微电解化学催化固体颗粒与天然生物质丝瓜络的耦合作用结果,且系统具有pH缓冲作用,可使其处在有利于硝态氮脱除的状态。因而此技术对脱除地下水中硝酸盐氮是高效、可行的,为地下水深度脱氮提供了新工艺、新思路。(来源:环境工程学报 作者:李德生)