N-亚硝胺(NAs)是一类带有亚硝基功能团的化合物, 已知的NAs超过300多种, 其中大多数NAs呈现出诱变性和致癌性.国内外研究报道比较多的NAs主要有9种:N-亚硝基二甲胺(NDMA)、N-亚硝基二乙胺(NDEA)、N-亚硝基甲乙胺(NMEA)、N-亚硝基二丁胺(NDBA)、N-亚硝基哌啶(NPIP)、N-亚硝基吗啉(NMOR)、N-亚硝基吡咯(NPYR)、N-亚硝基二丙胺(NDPA)和N-亚硝基二苯胺(NDPhA).这类化合物的水溶性较大(表 1), 所以它们在环境水体中普遍存在且频繁检出, 包括饮用水、污水、河水甚至地下水中, 检出质量浓度一般为几至几十ng・L-1, 个别化合物(如NDMA)可高达几百ng・L-1.环境水体中NAs的来源比较广泛, 人类日常生活和大多数工业活动都会产生和排放NAs, 包括生活废水的排放, 饮用水和污水的消毒处理, 以及食品、化妆品、橡胶制品、聚合材料、染料等产品的加工使用等, 其中关注比较多的是饮用水消毒过程中NAs的产生, 尤其是检出频率较高且致癌性较强的NDMA.据报道, NDMA的致癌风险远高于其他卤代消毒副产物(如三卤甲烷和卤乙酸), 当致癌风险水平为10-6 ng・L-1时, NDMA致癌风险剂量为0.7 ng・L-1(三氯甲烷为6 000 ng・L-1).为了减少饮用水中NDMA对人体的暴露风险, 世界卫生组织(WHO)规定的饮用水中NDMA的最大允许摄入量为100 ng・L-1, 美国加利福尼亚州和马萨诸塞州规定饮用水中NDMA的控制标准为10 ng・L-1.

表 1 6种NAs的基本信息及其在水样中的方法回收率、检出限(LOD)和定量限(LOQ)
最近十来年, 我国学者开展了许多有关NAs的调查研究, 大多数研究主要集中在食品和饮用水中NAs的浓度水平调查、橡胶制品中NAs的释放量调查、以及饮用水处理过程中NAs的降解去除.2016年, 张秋秋等利用近几年我国饮用水水质调查的NDMA数据, 并结合疾病模型, 对我国城市饮用水中NDMA的健康风险进行估算得出:我国饮用水中NDMA的安全标准应为6.12 ng・L-1, 但我国暂未确定NDMA在饮用水中的控制标准.同年, 清华大学环境学院陈超课题组发表的研究成果表明:在全国23个省、44个城市(城镇)、155个点位采集的164个水样(包括出厂水、龙头水和水源水)中普遍检出9种常见的NAs, 它们在出厂水和龙头水中的检出率远高于美国; 9种NAs中NDMA质量浓度最高, 出厂水和龙头水中NDMA的平均质量浓度分别为11 ng・L-1和13 ng・L-1, 水源水中的NDMA生成潜能平均为66 ng・L-1; 在长江流域的水样中, 9种NAs检出的质量浓度更高, 出厂水和龙头水中NDMA的平均质量浓度分别为27 ng・L-1和28.5 ng・L-1, 水源水中的NDMA生成潜能平均为204 ng・L-1.可见, 我国水源水中NAs污染状况较为严重和普遍(尤其是NDMA), 对人体存在较高的健康风险.大量研究表明, 生活污水偷排(或直排)以及污水处理厂出水排放是水源水中NAs的一个重要来源.然而, 目前有关我国污水处理厂中NAs的分布和去除的研究比较少见, 且有限报道中的多数只关注NDMA, 因此有必要系统地探讨NAs在我国污水处理厂中的分布及其去除规律.
本研究在广州选择了3种不同处理工艺的污水处理厂, 采集每个工艺段的污水样及其尾水排放口上下游河流的河水样, 测定其中NDMA、NPIP、NMOR、NPYR、NDEA和NMEA这6种NAs的质量浓度水平, 系统研究了NAs在不同处理工艺污水处理厂各工艺段的分布及其去除规律, 并分析了受纳河水中NAs的质量浓度分布及其来源.研究结果有助于揭示NAs在我国污水处理厂各工艺段的分布及其去除规律, 以期为优化污水处理工艺、提高污水处理厂对NAs及其前驱物的去除效率提供理论基础.
1 材料与方法
1.1 试剂与仪器
标准品NPIP(99.2%)、NMOR(99.0%)、NPYR(99.0%)、NDEA(99.5%)购置于德国Dr. Ehrenstorfer公司; NDMA(98.0%)和NMEA(99.5%)购置于美国O2Si公司; 同位素内标NDMA-d6(99.0%)购置于挪威Chiron公司.
甲醇(色谱纯)和二氯甲烷(色谱纯)购置于德国Merck公司; 甲酸(色谱纯)购于美国Tedia公司; 硫代硫酸钠(99.0%)和碳酸氢钠(分析纯)购置于美国SIGMA公司.HLB固相萃取小柱(200 mg, 6 mL)购置于美国Waters公司; 椰壳活性炭固相萃取小柱(2 g, 6 mL)购置于美国Supelco公司.玻璃纤维滤膜(GF/F, 0.70 μm)购置于英国Whatman公司; 有机相尼龙过滤器(13 mm × 0.22 μm)购置于上海安谱实验科技股份有限公司.
固相萃取装置(16孔)购置于美国Alltech公司; MTN-2800D氮吹仪购置于天津奥特赛恩斯仪器有限公司; 1200系列超高效液相色谱串联G6460A三重四级杆质谱仪(UHPLC-MS/MS)购置于美国Agilent公司.实验用水由Milli-Q超纯水仪(美国Millipore公司)制取.
1.2 采样点设置及水样采集
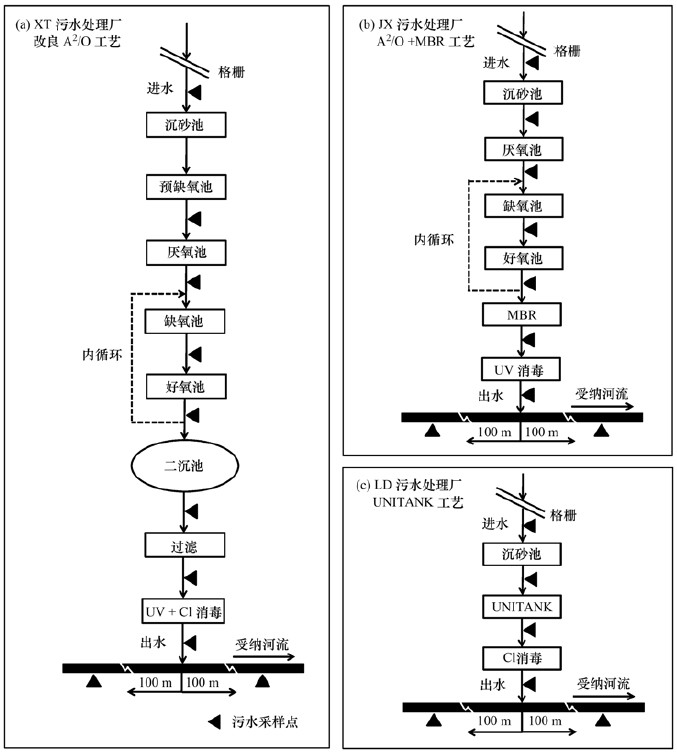
本研究选择的3个不同处理工艺的生活污水处理厂位于广东省广州市, 代号分别为XT、JX和LD, 所采用的处理工艺分别为改良A2/O、A2/O+膜生物反应器(MBR)和组合交替式活性污泥法(UNITANK).采样点设置于每个污水处理厂各工艺段的出水口处及其尾水排放口上下游河流100 m处, 各处理工艺的流程及其对应的采样点位如图 1所示.样品采集于2015年5~10月进行, 分别采集各工艺段污水样品3次作为24 h混合样于1 L棕色瓶中, 每次采样体积大致相当, 每个点位均采集3个平行样; 而河水样品则在污水处理厂采样当天中午采集一次, 采样体积为1 L, 同样采集3个平行样.每个平行样(1 L)加入100 mg硫代硫酸钠去除水样中可能存在的余氯.另外, 为了考察不同污水处理工艺对常规污染物的去除情况, 还对每个污水处理厂额外采集了一份进水和出水(各1 L), 用于基本水质参数测定.所有样品储存在放有冰袋或冰盒的保温箱中运回实验室存放于4℃冷库, 48 h之内进行前处理.
图 1
1.3 水样前处理
运回实验室的水样采用固相萃取(SPE)的方法对NAs进行提取和净化, 采用的固相萃取柱为HLB柱(上)串联椰壳活性炭柱(下).每个水样(1 L)都采用70 mm GF/F滤膜进行抽滤, 滤液分别转入1 L样品瓶中, 加入1 mg・L-1内标(NDMA-d6)100μL, 再加入2 g NaHCO3调节水样pH至8.0左右, 混匀, 以约10 mL・min-1的流速载入活化后的固相萃取串联柱(依次加入2×5 mL二氯甲烷+2×5 mL甲醇+2×5 mL Milli-Q水进行活化).上样完毕后, 每个瓶子加入10 mL Milli-Q水进行润洗, 分两次转入串联柱中进行淋洗.然后在负压下抽干串联柱, 分别加入4×5 mL二氯甲烷进行洗脱, 洗脱完毕后, 在洗脱液中分别加入1 mL Milli-Q水, 于室温下用缓慢的氮气流浓缩, 约0.5 mL时取出, 采用含20%甲醇的水溶液定容至1 mL.最后采用0.22 μm有机相针式滤膜过滤至棕色进样瓶中, 于-20℃冰柜中保存待测.
1.4 仪器分析
水样提取液中的NAs采用配有电喷雾离子化检测器(ESI)的UHPLC-MS-MS在正离子模式下进行测定, 扫描方式为多反应监测(MRM)模式, 采用内标法进行定量.仪器分析采用的色谱柱为Zorbax SB-C18 (100 mm×3 mm, 1.8 μm), 柱温40℃; 流动相A为甲醇, B为含0.05%甲酸的水溶液(超纯水), 梯度洗脱程序为:0~4 min 20%~40%A, 4~5 min 40%~95%A, 5~7.5 min 95%A, 7.5~8.5 min 95%~20%A, 流速0.3 mL・min-1, 进样体积30μL; 干燥气温度350℃, 干燥气流量10 mL・min-1, 雾化器压力413.7 kPa, 电喷雾电压500 V.NAs及内标的各项质谱采集参数采用Optimizer软件(美国Agilent公司)优化得到.
水样提取液中的化学需氧量(COD)、5日生化需氧量(BOD5)、氨氮(NH4+-N)、总氮(TN)和总磷(TP)采用常规水质分析方法进行测定.
1.5 质量保证和质量控制
本研究设置了添加回收率实验(3个平行)以考察分析方法的准确度和精密度, 分别在河水、污水处理厂进水和出水中添加NAs混合标样, 使得每个目标化合物的添加质量浓度均为100 ng・L-1, 分别按照1.3节和1.4节描述的方法进行前处理和仪器分析.然后根据测定结果计算方法回收率, 并基于信噪比计算方法检出限(LOD)和定量限(LOQ), 方法回收率、检出限和定量限基本满足测定要求(表 1).在数据分析时, 居于LOD和LOQ之间的数据以1/2 LOQ计算, 低于LOD的数据以0计算.
样品前处理和仪器分析过程中执行严格的质量保证和质量控制.每一批样品进行前处理时, 均采用Milli-Q水增设1个空白对照样和3个加标控制样(添加质量浓度为100 ng・L-1), 以考察前处理过程是否规范、准确; 对每一批前处理样品进行仪器分析时, 均需重新配制并测定NAs的混合标准工作溶液(每个目标化合物的质量浓度梯度均为:2、5、10、30、60和100 μg・L-1), 同时穿插测定溶剂空白和60 μg・L-1的混合标准溶液, 以考察是否存在背景污染及仪器运行状况是否正常.所有样品前处理和仪器分析过程未发现异常.具体联系污水宝或参见http://www.dowater.com更多相关技术文档。
2 结果与讨论
2.1 不同处理工艺污水处理厂对常规污染物的去除
3个不同处理工艺污水处理厂对COD、BOD5、NH4+-N、TN和TP这5种常规污染物的去除效果见表 2.总体看来, A2/O+MBR和UNITANK工艺对5种常规污染物的去除效果都较好(去除率均大于71%), 平均去除率分别为84%和82%, 出水水质可以达到国家《城镇污水处理厂污染物排放标准》(GB 18918-2002)中的一级A排放标准.而改良A2/O工艺对COD、BOD5、NH4+-N、TN的去除效果较好(去除率均大于62%), 出水水质可以达到GB 18918-2002中的一级A排放标准; 但对TP的去除效果一般(去除率为43%), 但出水水质可以达到GB 18918-2002中的一级B排放标准.由此可推知, 本研究选择的A2/O+MBR、UNITANK和改良A2/O这3个工艺的污水处理厂在采样期间是正常运行的.

表 2 不同污水处理工艺对常规污染物的去除情况
2.2 NAs在不同处理工艺污水处理厂中的质量浓度分布
NDMA、NPIP、NMOR、NPYR、NDEA和NMEA这6种NAs在不同处理工艺污水处理厂中的质量浓度分布见图 2.从中可见, 在XT污水处理厂中[图 2(a)], 6种NAs在各工艺段的所有水样(n=24)中均有检出, 但各化合物质量浓度差异较大, 其中NPIP和NDMA质量浓度水平较高, 尤其是NPIP, 其在进水中的质量浓度高达825.73 ng・L-1; 在JX污水处理厂中[图 2(b)], 只有NMEA未检出(
图 2
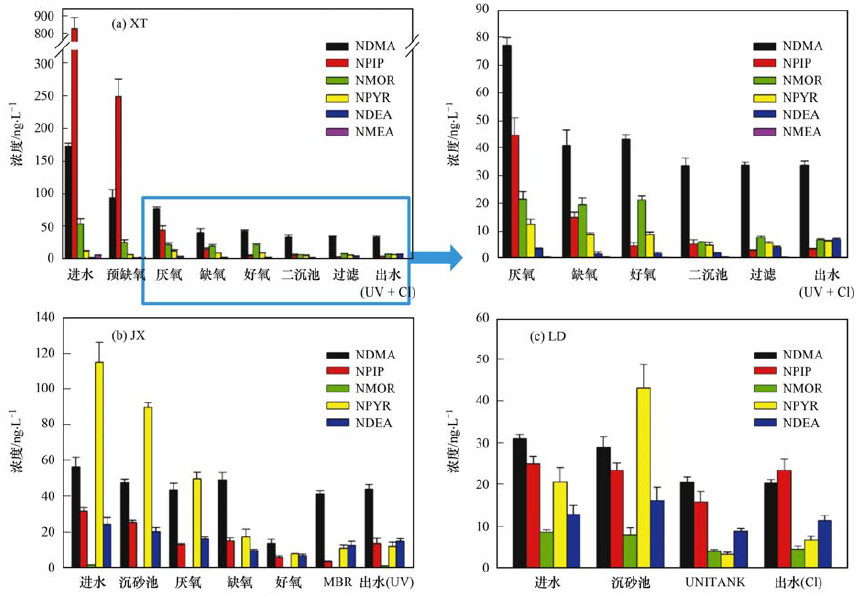
图 2 6种NAs在3个污水处理厂各工艺段废水中的质量浓度分布
2.3 NAs在不同处理工艺污水处理厂中的去除
NDMA、NPIP、NMOR、NPYR、NDEA和NMEA这6种NAs在不同处理工艺污水处理厂中的去除情况见图 3.由图 3(a)可见, 3个不同处理工艺污水处理厂对NAs的去除率差异较大:XT污水处理厂(改良A2/O)对NDMA、NPIP、NMOR和NMEA这4种NAs的去除率大于80%, JX污水处理厂(A2/O+MBR)对NPIP和NPYR这2种NAs的去除率大于55%, LD污水处理厂(UNITANK)仅对NPYR的去除率大于65%, 其余未列出NAs在3个污水处理厂中的去除率均小于50%, 大多数NAs的去除率与前人报道的数值基本一致.3个不同处理工艺污水处理厂对∑6NAs的去除率排序为XT(改良A2/O, 95%)>JX(A2/O+MBR, 63%)>LD(UNITANK, 32%), 这个排序和6种NAs在3个污水处理厂废水中的质量浓度水平排序一致(图 2), 表明污水处理厂对NAs的去除率除了与工艺类型及其运行效果有关, 还与污水处理厂的进水属性密切相关, 尤其是NAs及其前驱物在进水中的质量浓度水平.另外, 3种处理工艺中, 改良A2/O工艺(XT)对∑6NAs的去除效果最好(去除率95%), 而对常规污染物的去除效果却最差(平均去除率71%, 表 2); UNITANK工艺(LD)对∑6NAs的去除效果最差(去除率32%), 而对常规污染物的去除效果却不错(平均去除率82%, 表 2), 暗示了同一污水处理工艺对NAs和常规污染物的去除机制是有区别的.
图 3
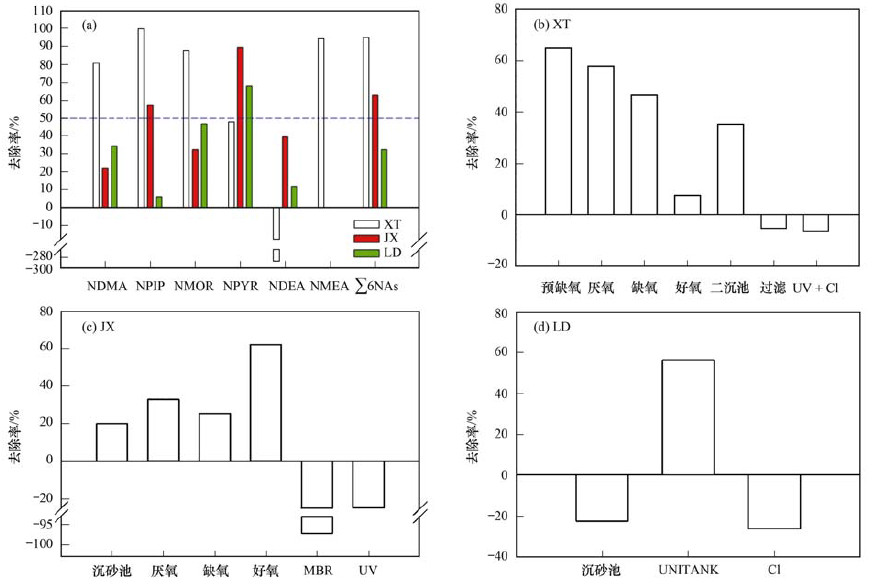
为了探索不同污水处理工艺对NAs的去除规律, 本研究还分析了3个不同处理工艺污水处理厂各工艺段对∑6NAs的去除情况[图 3(b)~3(d)].在XT污水处理厂(改良A2/O)中[图 3(b)], 对∑6NAs发挥了较好去除作用的是预缺氧、厌氧和缺氧段, 去除率分别为65%、58%和46%;而过滤和UV+Cl消毒阶段对∑6NAs的去除率分别为-5%和-6%.在JX污水处理厂(A2/O+MBR)中[图 3(c)], 主要是好氧段对∑6NAs的去除发挥了主要作用, 去除率为62%;而MBR和UV消毒阶段对∑6NAs的去除率分别为-97%和-25%.在LD污水处理厂(UNITANK)中[图 3(d)], 只有UNITANK阶段对∑6NAs的去除率为正值(56%); 而沉砂池和Cl消毒阶段对∑6NAs的去除率均为负值(分别为-22%和-26%).总体而言, 不同污水处理工艺对NAs的去除主要发生在生化阶段, 说明微生物的降解和转化对废水中NAs的去除发挥了重要作用, 这与前人的研究结果一致.沉砂、过滤、MBR和消毒阶段呈现的NAs质量浓度反升现象, 可能原因主要有两个:一是污水处理厂进水水质波动较大而水力停留时间较长, 从而导致了NAs质量浓度反升(XT、JX和LD污水处理厂的水力停留时间分别为12.5、9.5和13 h); 二是废水处理体系中的一些NAs前驱物经一系列反应后形成了NAs.对于消毒阶段, 许多研究结果已经证实NAs前驱物经Cl、UV+Cl消毒后会形成NAs, 对于过滤和MBR阶段, 过滤材料、MBR材料及废水中的NAs前驱物会与加入的清洗药剂反应后形成NAs.据报道, JX污水处理厂使用MBR膜清洗药剂为酸、碱和NaClO, 酸和NaClO在废水中反应后可产生Cl2和HClO, 相当于经历了Cl消毒阶段.
2.4 受纳河水中NAs的质量浓度分布及其来源分析
本研究对比了不同处理工艺污水处理厂进出水及其尾水排放口上下游河水中NAs的质量浓度分布情况(图 4), 以进一步分析受纳河水中NAs的来源.由图 4可见, 6种目标NAs在XT、LD和JX污水处理厂的受纳河流中普遍存在[除NMEA外, 其余化合物的检出率均为100% (n=6)], 它们在对应河流河水样品中的质量浓度范围分别为0.47~203.64(NDMA)、< LOD~23.47(NDMA)和 < LOD~41.43(NPYR)ng・L-1, 其中主要污染物为MDMA、NPIP和NPYR, 和污水处理厂进水中的主要污染物一致; 受纳河水中∑6NAs的质量浓度上游高于下游, 且高于污水处理厂出水(LD除外), XT污水处理厂尤为明显(位于工业集中区); ∑6NAs在3个污水处理厂进水及其受纳河水中的质量浓度呈现出明显的正相关关系:进水中∑6NAs质量浓度越高的污水处理厂, 其对应受纳河水(不论上下游)中∑6NAs质量浓度也越高.综合上述现象可推知:污水处理厂出水是受纳河流中NAs的来源之一, 其他来源还包括未经处理的生活污水和工业废水以及工业区地表径流等的汇入, Lee等对韩国釜山污水处理厂及其受纳水环境的调查研究也揭示了这一规律.因此, 为了减少NAs向受纳河流的输入, 应该从家庭、工厂等产生源头上减少NAs及其前驱物的使用和排放, 同时增强污水收集和处理能力、优化污水处理工艺, 进一步提高污水处理厂对NAs及其前驱物的去除效率.
图 4

3 结论
(1) 6种NAs(NDMA、NPIP、NMOR、NPYR、NDEA和NMEA)在我国广州3种不同处理工艺污水处理厂各工艺段废水中普遍存在, 其中主要污染物为NPIP、NDMA和NPYR.
(2) 3种不同处理工艺的污水处理厂都能对NAs起到一定的去除效果, 其中改良A2/O和A2/O+MBR对NAs的去除效果较好; 生化阶段的微生物的降解和转化对NAs的去除发挥了主要作用, 而过滤、MBR和消毒阶段, 废水处理体系中NAs前驱物经一系列反应后会形成一定的NAs增量.
(3) 污水处理厂出水对受纳河流中NAs的输入具有一定贡献, 但未经处理的生活污水和工业废水以及工业区地表径流的汇入也要引起重视.(来源:环境科学 作者:柳王荣)


