水和油是2 种不相容的物质,为使水分散到油中,通常会使用到乳化剂,使不相容的油水两相发生乳化形成稳定的乳化液。由于生成的乳化液体系极为稳定,因此被广泛应用于机械加工工业、汽车发动机加工流水线、冷轧钢板厂的轧锟及钢板的冷却和润滑。通常,使用一段时间后的乳化液会老化变质,性能下降,由此对乳化液进行更换,形成乳化液废水。由于乳化液废水油水混合十分均匀,因此,对其的处理应首先实现油水的分离,即破乳。目前,国内外常用的破乳方法包括化学药剂破乳法、酸化破乳法、超声波破乳法和超滤破乳法等,其中酸化破乳法,主要是加酸将乳化液调节至酸性,利用H+ 的作用中和油滴表面覆盖的带负电荷的双电层,使得油水界面的表面活性剂游离出来,从而破坏体系的稳定性,达到油水分离的目的。由于该方法仅使用无机酸做破乳剂,因此操作较为简便、价格较为经济,用于乳化液破乳具有一定优势。但酸化破乳法仅适用于由阴离子表面活性剂组成的乳化液体系,加之对一些稳定性极好的乳化液破乳效果不够理想,限制了其应用。另一方面,研究表明,乳化液体系温度会影响乳化液体系的稳定性,当体系温度升高时,会增加分子的热运动,利于液珠的聚结,同时温度升高可使油相黏度降低,使得油水界面膜减弱,利于破乳。为研究加热破乳的效果,傅大放等用微波辐射和电炉加热乳化液进行对比研究,表明微波辐射能显著降低乳化液的Zeta 电位,达到了较理想的破乳效果。此外,还有学者将加热法用于化学破乳,研究表明,加热对化学破乳效果有促进作用。
但从目前已有的文献来看,很少有人将酸化和加热联用,用于乳化液破乳。同时,在实际工程中,对于一些稳定性极佳的乳化液废水,采取单一的方法进行破乳往往效果不佳。因此,笔者在乳化液处理的工程小试中将加热法和酸化法联用,以考察加热和酸化过程联合的破乳效果。同时,由于加热酸化法仅实现了油水的分离,因此破乳后的出水仍具有较高的污染负荷,且可生化性较差,不利于后续生化处理,故考虑采取Fenton 氧化进行进一步处理。
1 实验部分
1.1 实验废水
实验所用废水为成都某电子制造商生产车间废弃产生的乳化液,所用乳化剂为日本进口,主要成分是阴离子表面活性剂,为O/W 型乳化液。原水为乳白色,初始COD>20 万mg/L,浊度> 8 000 NTU,含油量约为15%,pH 在8 左右。
1.2 试剂和仪器
试剂: 98% 浓硫酸; 30% H2O2; FeSO4・7H2O;NaOH,所用药品均为分析纯。仪器: 雷博4050 型COD 恒温加热器; WGZ-500B 型浊度计; PHS-3D 型pH 计; QYC-211 型全温空气摇床; OxiTop IS 6 型BOD 仪; 恒温水浴锅。
1.3 实验方法
1.3.1 酸化破乳
在500 mL 锥形瓶中盛装200 mL 废水,加入一定量的浓硫酸使废水酸化pH 降低,再将其放入恒温水浴锅,进行水浴加热。加热完后,取废水油层下的水层,测COD、浊度、油类含量及pH。
1.3.2 Fenton 氧化
取酸化破乳后油层下的清液100 mL 加入250mL 锥形瓶,加入NaoH 调节废水pH 后,依次投加一定量FeSO4・7H2O 和30% H2O2,静置10 min 后放入摇床振荡2 h,摇床条件控制为温度恒定25℃、转速恒定150 r/min,振荡完毕后,取出锥形瓶静置隔夜,测COD 及BOD5。
2 实验结果及分析
2.1 加热酸化破乳
2.1.1 加热温度对破乳效果的影响
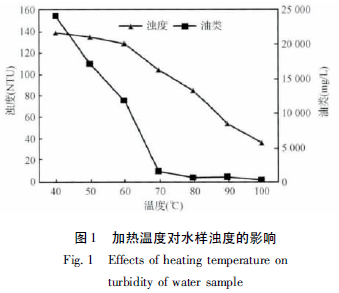
在加酸量为1.0 mL 98% H2SO4/100 mL 乳化液条件下,加酸后的乳化液在常温状态下仍保稳定。在加热时间2 h 条件下,分别将加热温度控制在(40±1)℃、(50±1)℃、(60±1)℃、(70±1)℃、(80±1)℃、(90±1)℃、(100±1)℃,随着加热温度的升高,体系稳定的乳化液逐渐出现了油水界面的分离,下层为具有一定浊度的黄色水层,中间层为灰白色的乳化剂层,上层为油层。随着温度的升高,水层的厚度不断增大,油水分离效果更为明显,在100℃处水层厚度达到最大。下层水样测浊度发现,在40~60℃时,下层水样浊度基本无变化且浊度较高,在70~100℃时,下层水样浊度显著降低,同时下层水样测油类含量发现,在70℃前油类含量处于较高水平,但当加热温度大于70℃时油类含量大大降低,如图1 所示。由此推断,在70℃以下时加热温度不足以完全破坏油水界面的界面膜,使得水相中仍溶解了部分油类物质,但当加热温度大于70℃时,由于液珠的聚结和油相粘度的进一步降低,油水界面的界面膜强度大大降低,所以随着温度的提高,油水分离过程进行较快。因此,在加热温度100℃时,可以获得良好的破乳效果,但是考虑到100℃时乳化液水相在沸腾过程中蒸发较快,因此将加热温度控制在95℃较佳。
2.1.2 加热时间对破乳效果的影响
除加热温度外,加热时间也是影响加热酸化破乳程度的重要因素。在加热状态下,乳化液在热力学上表现出不稳定性,因此实现较为彻底的破乳只是时间问题。为此,在加酸量为1.0 mL 98%H2SO4/100 mL 乳化液、加热温度95℃条件下,在不同加热时间条件下对乳化液进行破乳处理,结果如图2 所示。可以看出,破乳后下层水样的浊度总体呈下降趋势,在0.5 h 处为81.9 NTU,浊度较高,其余浊度均在43.2 NTU 以下。因此认为,加热时间大于1 h 即可获得较好的破乳效果。

同时,测定水层COD 发现,其呈先升后降的趋势,在0.5~1.5 h,COD 先升高,在2~5 h,逐渐下降。出现这一趋势,可能是因为加热酸化过程中的无机酸加入使得阴离子表面活性剂转化为电中性的有机酸(部分能溶于水、部分不溶于水),同时乳化剂含有很多成分复杂的助剂,因此生成产物非常复杂,一部分生成物不溶于水,悬浮形成灰白色的中间层,另一部分溶于水中表现为COD,而在0.5~1.5h,加热促进了溶于水的这部分COD 的生成,导致COD 升高,但总的来说,随着加热时间的增长,下层水中的油相慢慢分离溶出,使得COD 表现为下降趋势。最后,考虑到1 h 加热时间,已能将下层水层浊度降低到较低水平,具有较好的破乳效果,因此将加热时间控制在1 h,以取得较低能耗。
2.1.3 加酸量对破乳效果的影响
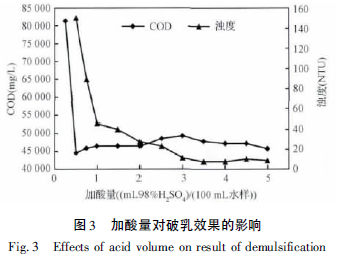
无机酸的加入能将表面活性剂转化为电中性的有机酸,破坏乳化液的稳定性,因此加酸量对乳化液破乳效果有非常大的影响,特别是在加酸量不足的情况下,如图3 中的加酸量为0.25、0.5 和0.75 mL98% H2SO4/100 mL 乳化液的实验组,其浊度都处于较高水平,特别是加酸量0.25 mL H2SO4/100 mL乳化液的实验组,其浊度> 3 000 NTU,由此可见加入的浓H2SO4基本未起到任何作用,同时进行的加热处理也不能对乳化液的稳定性造成影响。但随着加酸量的增多,乳化液的浊度逐渐下降,最低点在加酸量为4.0 mL H2SO4/100 mL 乳化液达到最低点8NTU。
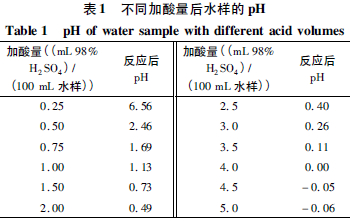
同时,其COD 呈先增后降的趋势,在加酸量为3.0 mL H2SO4/100 mL 乳化液时COD 最高,造成这一情况的原因类似于加热时间对破乳效果的影响,加酸量的增加使得反应产物溶于水中的COD 增多,但由于破乳过程总体向着油水彻底分离的过程进行,因此下层水样中COD 最终表现出下降趋势。因此,认为加酸量在4.0~5.0 mL H2SO4/100 mL 乳化液时,具有最好的破乳效果,但是考虑到加酸量的增多使得反应后溶液的pH 过低(如表1 所示),会造成后续中和所投加的中和剂药剂用量增大,以及后续的厌氧处理SO42-浓度过高的问题,因此将加酸量控制在1.0 mL 98% H2SO4/100 mL 乳化液,同样可以获得较为理想的破乳效果。
综上,将加热酸化的反应条件控制在加酸量1.0 mL 98% H2SO4/100 mL 乳化液、加热温度95℃、加热时间1 h,最终初始COD>20 万mg/L,浊度> 8 000 NTU,含油量约为15% 的乳化液在该条件下,COD 降低为46 592 mg/L,浊度20 NTU,COD和浊度的去除率分别达到了76.7%和97.5%以上。
2.2 Fenton 氧化
2.2.1 初始pH 对Fenton 氧化效果的影响
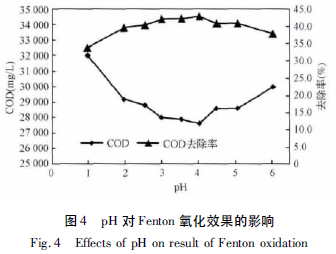
取经上述条件破乳后的乳化液废水进行Fenton氧化,控制加入废水的H2O2和Fe2+分别为ρ(H2O2)/ρ(COD)=1.0、ρ (Fe2+)/ρ (COD)=0.04,在不同的pH 条件下进行反应,结果如图4 所示。从图中可以看出在pH 为2~5 之间时,Fenton氧化都具有较高的COD 去除率,且在pH=4 时具有最好的催化氧化效果。但从整体来看,pH 对Fenton 氧化去除效率影响较小,去除率在33.6%~42.8%之间波动,绝大部分位于39.4%~42.8% 之间,这主要是由于在Fenton 反应中H+的作用主要是为・OH的产生提供一个酸性环境,仅会影响Fenton氧化的反应速率,并且从反应后的废水pH 来看(如表2 所示),其pH 最终都会降低到一定水平,因此Fenton 反应过程只要有一定量的H+即可保证反应所需的酸性环境,就能够使反应进行下去,因此认为选择pH=4 足以满足Fenton 反应所需H+且在去除率上最优。具体参见http://www.dowater.com更多相关技术文档。
2.2.2 Fe2+和H2O2对Fenton 氧化效果的影响
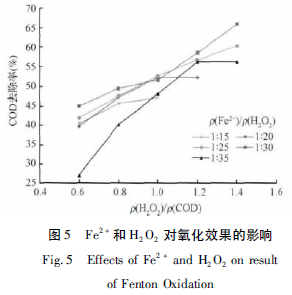
Fe2+和H2O2的投加量是Fenton 氧化最为关键的2 个参数,在对破乳后的乳化液废水处理中,分别将ρ(H2O2)/ρ(COD) 控制在0.6、0.8、1.0、1.2、1.4和1.6,在Fe2+投加量分别为ρ(Fe2+)/ρ(H2O2) =1∶15、1∶20、1∶30、1∶35,pH=4 的条件下进行反应,结果如图5 所示(无数据点为反应过于激烈废水爆沸喷出) 。首先,废水COD 的去除率都随着H2O2投加量的增多而增大,但是随着ρ(Fe2+)/ρ(H2O2)的增大,反应趋于过度激烈,不利于正常进行; 其次,在反应正常进行的情况下,整体上COD 去除率随着ρ(Fe2+)/ρ(H2O2) 的减小而增大,但是当ρ(Fe2+)/ρ(H2O2)=1∶35 时,反应COD 去除率反而降低。这可能是因为由于Fe2+在芬顿反应中只是作为催化剂,整个反应过程只需要少量Fe2+催化即可,ρ(Fe2+)/ρ(H2O2) 过高可能会导致Fe(OH)3的生成反应过快,Fe2+量减少,致使Fenton 反应活性链式反应终止; 而当ρ(Fe2+)/ρ(H2O2) 低于1∶30 时,体系没有足够的Fe2+催化,导致芬顿的链式反应不完全,从而去除效率较低。因此,将Fenton 反应控制在ρ(Fe2+)/ρ(H2O2)=1∶30、ρ(H2O2)/ρ(COD) =1.4、pH=4 的条件下,具有最优的Fenton 氧化效果,经处理后的出水COD 可降到18 600 mg/L,去除率达61.4%,其B/C 可由破乳后的0.11 提高到0.43,废水的可生化性大大提高。
3 结论
采取加热酸化-Fenton 氧化处理乳化液废水,可达到良好的破乳和处理效果,研究表明:
(1) 该方法可使初始COD>20 万mg/L,浊度>8 000 NTU 的乳化液废水COD 降到18 600 mg/L,浊度降到20 NTU 以下,COD 和浊度的去除率分别达90.7%和97.5%以上;
(2) 加热和酸化过程联合作用,使得破乳更易于发生,最佳反应条件为加酸量1.0 mL 98%H2SO4/100 mL 乳化液、加热温度95℃、加热时间1h 时,破乳效果良好;
(3) Fenton 氧化处理破乳后的乳化液,在ρ(Fe2+)/ρ(H2O2)=1∶30、ρ(H2O2)/ρ(COD)=1.4、pH=4 的条件下,能进一步去除61.4% 的COD,同时使废水B/C 由破乳后的0.11 提高到0.43,生化性大大提高。
仍需指出的是,为实现乳化液废水的达标排放,应对Fenton 出水进行进一步处理,考虑到其污染负荷仍较高,但生化性已大大改善,因此可考虑采用厌氧+ 好氧联合工艺进行处理。此外,加热酸化破乳过程会向废水体系引入大量的H+和SO42-,导致Fenton 反应进水需调整pH,同时过高的SO42-可能给后续进行的厌氧反应造成麻烦,因此应考虑减少H2SO4的使用量,可在后续的实验中采用多种无机酸混合投加的形式或使用少量强电解质配合H2SO4进行破乳,在保证破乳效果的前提下,减少H+和SO42-的用量。


