与传统脱氮工艺相比, 厌氧氨氧化工艺具有脱氮途径短、节省曝气量、无需外加碳源、污泥产量少等优点[1], 已成为目前最具前景的污水脱氮工艺[2].
厌氧氨氧化以亚硝化工艺为基础.亚硝化工艺难以控制, 出水中含有较高浓度的硝氮[3, 4].同时, 厌氧氨氧化工艺将污水中的氨氮和亚硝氮转化为氮气和少量硝氮, 极限脱氮效率为89%[5], 且无法去除进水中固有的硝氮, 因此在实际应用中整体工艺的出水氮素浓度偏高[6].随着污水排放标准日益严格, 提高氮素去除率也迫在眉睫.有文献指出, 采用厌氧氨氧化耦合反硝化的方法可以有效地提高反应器的总氮去除率[7~9], 但国内外对SAD工艺的研究停留在配水上[10~12], 实际应用极少.
亚硝化工艺出水中, 可降解有机物浓度较小, 后续的SAD工艺往往需要外加碳源.碳源对SAD工艺有重要的影响[13~15].污水处理厂通常投加的有机碳源为甲醇、丙酸钠和葡萄糖等[16].甲醇会对厌氧氨氧化菌产生不可逆的抑制作用, 不适合作为SAD工艺的有机碳源[17].丙酸钠和葡萄糖对厌氧氨氧化菌抑制作用较小[18], 理论上可以作为SAD工艺的碳源, 但在实际工程应用中尚未有人研究.
本试验在污水处理厂进行, 利用A/O除磷和亚硝化工艺处理后的实际生活污水为基质, 分别投加葡萄糖和丙酸钠启动SAD工艺, 研究实际工程应用中有机碳源对SAD工艺的影响.
1 材料方法
1.1 试验装置
试验采用2个完全相同的上向流生物滤柱(图 1), 编号为1号和2号.反应器由有机玻璃制成, 内径20 cm, 承托层高5 cm, 滤料高50 cm, 有效体积15 L.滤柱每隔10 cm设置取样口, 承托层采用粒径为4~8 mm的砾石, 内部装填直径5~10 mm的火山岩填料, 为了避免生物膜过量增殖导致滤柱堵塞的问题, 在底部设曝气装置以进行气水反冲洗.整个反应器外部用黑色保温棉缠绕以避光和保温.
1.2 接种污泥和试验水质
反应器启动时接种5 L厌氧氨氧化絮状污泥, 污泥浓度为2 000 mg・L-1.厌氧氨氧化絮状污泥来自于稳定运行的厌氧氨氧化SBR反应器, SBR反应器总氮去除率稳定在85%左右, 总氮去除负荷为0.5 kg・(m3・d)-1.
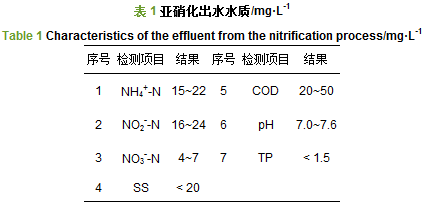
试验采用的基质为A/O除磷和亚硝化工艺处理后的实际生活污水, 具体水质如表 1所示.
1.3 试验方法
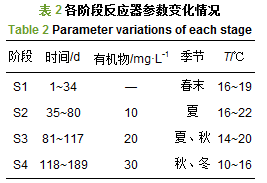
1号反应器进水中投加葡萄糖, 2号反应器进水中投加相同浓度的丙酸钠.根据基质中投加碳源浓度的不同, 反应器运行分为4个阶段, 各阶段运行参数如表 2所示.
S1阶段为厌氧氨氧化工艺启动阶段, 基质为A/O除磷和亚硝化工艺处理后的生活污水. S2~S4阶段为SAD工艺运行阶段, S2、S3和S4阶段分别投加10、20、30 mg・L-1有机物.
1.4 检测方法
水样分析中NH4+-N测定采用纳氏试剂光度法, NO2--N采用N-(1-萘基)乙二胺光度法, NO3--N采用紫外分光光度法, COD采用国标法测定(对水样进行预处理排除亚硝酸盐的影响), DO、pH和水温通过WTW便携测定仪测定, 其余水质指标的分析方法均采用国标方法.滤料表面生物膜厚度通过电子显微镜来精确测量[19].
反应速率的测定:从反应器取出滤料, 刮下生物膜解离并在烧杯中测定反应速率.烧杯设置机械搅拌, 测定厌氧氨氧化反应速率和反硝化反应速率.测定厌氧氨氧化反应速率时, 基质氨氮和亚硝氮浓度为50 mg・L-1, 调节碱度使碱度与氨氮之比为10, 温度控制在24~26℃, pH稳定在7.0~8.0, DO维持0.3 mg・L-1以下.测定反硝化反应速率时, 以150 mg・L-1甲醇作为碳源, 硝氮浓度为50 mg・L-1, 温度控制在24~26℃, pH稳定在7.0~7.8, DO维持0.3 mg・L-1以下.
2 结果与讨论 2.1 反应器的启动
污水处理厂厌氧氨氧化工艺在春季末期进行启动, 水温为15~19℃.启动时1号和2号反应器各接种5 L污泥浓度为2 000 mg・L-1的厌氧氨氧化絮状污泥.为了减少厌氧氨氧化污泥的流失, 启动初期对出水进行收集并循环进水.运行3 d后, 出水中SS浓度均小于20 mg・L-1, 絮状污泥已稳定截留在反应器中.此时将反应器改为连续流运行, 进入S1阶段.
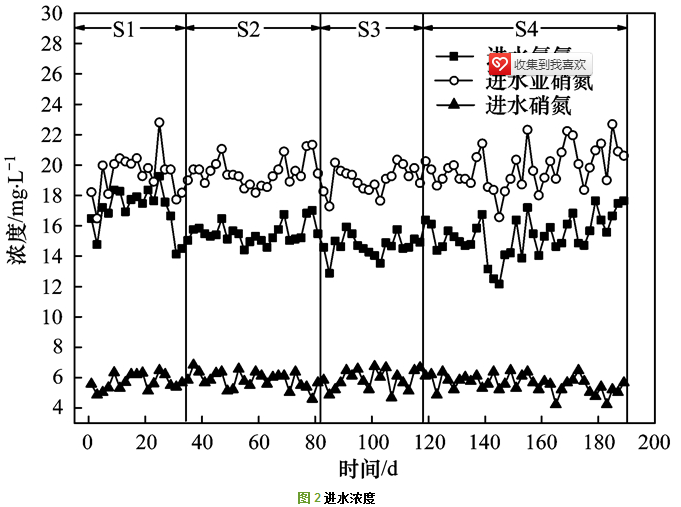
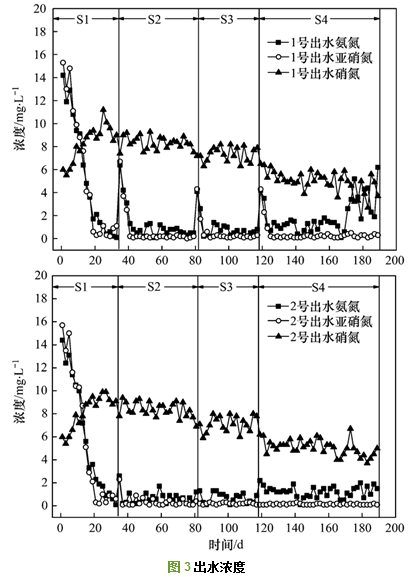
反应器启动时采用较低的水力负荷以减小厌氧氨氧化菌的流失, 滤速定为0.15 m・h-1, HRT约为5 h.进出水氮素浓度如图 2、3所示.从中可知, 随着反应器的运行, 出水氨氮和亚硝氮浓度逐步降低. 1号和2号反应器分别用19 d和25 d时, 使氨氮亚硝氮去除率大于90%, 完成了反应器的初步启动. 1号和2号反应器均在较短的时间内完成了厌氧氨氧化工艺的启动, 相较于其他研究成果[20, 21], 本试验反应器启动较快是由于接种了大量的厌氧氨氧化菌.第25~34 d时, 反应器氨氮、亚硝氮去除率大于95%, 1号反应器出水总氮浓度为9.6~13.4 mg・L-1, 2号反应器出水总氮浓度为9.8~12.6 mg・L-1, 均超过了北京市地方标准的A类排放标准.出水中氮素浓度主要以硝氮的形式存在, 一方面, 由于亚硝化工艺难以控制, 进水中硝氮浓度为4~7 mg・L-1; 另一方面, 厌氧氨氧化工艺会有少量硝氮产生, 因此导致出水含有大量硝氮.

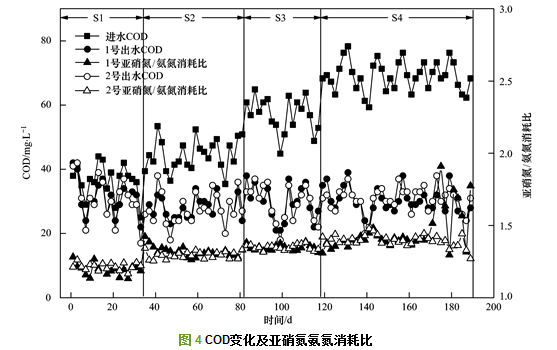
厌氧氨氧化反应方程式如式(1)所示[5].从中可知, 厌氧氨氧化菌按1.32:1的比例消耗亚硝氮和氨氮基质.总氮去除量和出水硝氮增量之比为8, 该值称为特征比.亚硝氮氨氮消耗比和特征比的大小受反硝化作用的影响, 反硝化作用增强, 亚硝氮氨氮消耗比和特征比均会上升.反应器亚硝氮氨氮消耗比如图 4所示.
S1阶段末期, 1号反应器平均亚硝氮氨氮消耗比为1.19, 平均特征比为8.18, 2号反应器平均亚硝氮氨氮消耗比为1.22, 平均特征比为8.76, 表明反硝化作用较弱. Kumar等指出[8], 高C/N比会使反硝化细菌取代厌氧氨氧化菌, 成为反应器的优势菌种.而在本试验中, S1阶段进水中COD浓度为25~50 mg・L-1, COD/NH4+为1.2~2, 处于较高水平, 但未观察到明显的反硝化作用. 1号和2号反应器出水COD维持在20~45 mg・L-1, COD去除率仅为10%~25%.原因是A/O工艺和亚硝化工艺出水中COD大多数为难降解的有机物[22], 反硝化菌缺少碳源, 活性处于较低水平.而难降解的有机物对厌氧氨氧化菌影响较小[23], 因此在厌氧氨氧化菌和反硝化菌的竞争中占据优势, 维持了厌氧氨氧化工艺的稳定.
2.2 SAD工艺的运行
S2阶段1号和2号反应器进水中分别有10 mg・L-1葡萄糖和丙酸钠, 启动SAD工艺. 1号反应器投加葡萄糖后, 氨氮和亚硝氮去除率从95%降低到60%左右, 运行6 d后, 氨氮和亚硝氮去除率恢复至90%以上. 2号反应器投加丙酸钠后, 氨氮和亚硝氮去除率从95%降低到80%, 运行2 d后, 氨氮和亚硝氮去除率恢复至95%以上, 丙酸钠对厌氧氨氧化菌的影响较小.第41~80 d, 1号反应器平均出水总氮浓度为9.16 mg・L-1, 2号反应器平均出水总氮浓度为9.33 mg・L-1. S2阶段1号反应器的亚硝氮氨氮消耗比为1.31, 平均特征比为12.60. 2号反应器的亚硝氮氨氮消耗比为1.29, 平均特征比为12.16. S2阶段末期, 1号和2号反应器处理效果几乎相同, 表明常温条件下, 低浓度葡萄糖和丙酸钠对于稳定运行的SAD工艺宏观作用效果相似.
S3阶段基质中有机物浓度提高到20 mg・L-1, 其他参数保持不变.在S3阶段初期, 1号反应器氨氮去除率由97%降低至78%, 厌氧氨氧化菌活性受到了暂时的抑制, 运行3 d后, 氨氮和亚硝氮去除率大于98%. 2号反应器氨氮去除率几乎没有变化.相比于S2阶段, 反应器用较短的时间恢复了高效的氨氮和亚硝氮去除效果, 抗有机物冲击负荷得到了明显的提升.第85~117 d, 1号反应器出水总氮浓度为6.5~9.8 mg・L-1, 平均出水总氮浓度为8.10 mg・L-1. 2号反应器出水总氮浓度为7.0~9.5 mg・L-1, 平均出水总氮浓度为7.98 mg・L-1.相较于厌氧氨氧化工艺, 此时SAD工艺将出水总氮浓度降低了26%.
S3阶段1号反应器亚硝氮氨氮消耗比上升至1.34, 特征比上升至21.92. 2号反应器亚硝氮氨氮消耗比为1.35, 平均特征比为25.51.亚硝氮氨氮消耗比及特征比的升高, 表明硝化细菌作用进一步得到提高.反应器保持着高效厌氧氨氧化活性的同时, 提高了反硝化菌的活性.根据厌氧氨氧化方程式计算[5], 厌氧氨氧化途径的氮损约为90%, 反硝化氮损约占10%.
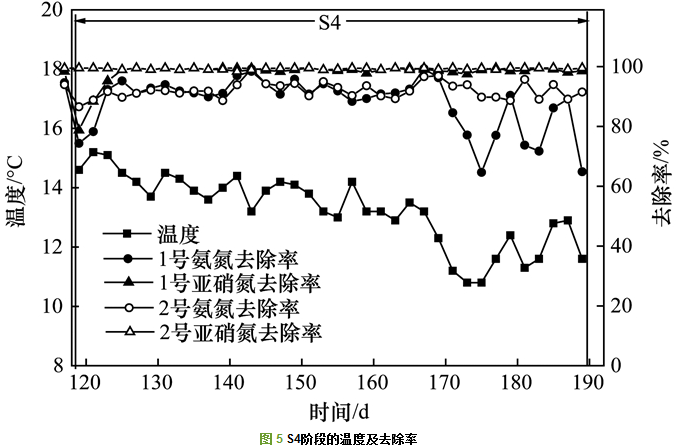
S4阶段, 进水中的有机物浓度提高到30 mg・L-1.该阶段进水温度、氨氮亚硝氮去除率如图 5所示.第123~170d, 水温为12.3~15.2℃, 1号出水总氮浓度为4.8~7.3 mg・L-1, 平均值为6.41 mg・L-1.与厌氧氨氧化工艺相比, SAD工艺出水总氮浓度降低了42%, 达到了北京市地方标准的A类排放标准.厌氧氨氧化和反硝化途径的氮损分别为83%和17%, 在常温条件下, 进水中投加30 mg・L-1葡萄糖, 厌氧氨氧化菌和反硝化菌耦合效果良好.第171d, 运行进入冬季, 进水温度降低至12℃以下. 1号反应器亚硝氮的去除几乎不受影响, 氨氮去除率明显下降, 且随温度变化而变化.进水温度为10~12℃时, 出水氨氮浓度为1.7~6.2 mg・L-1, 出水总氮浓度为7.0~10.2 mg・L-1, 超过了排放标准.研究表明, 厌氧氨氧化菌活性受温度影响大而反硝化菌活性受温度影响小[24].在本试验中, 基质中投加30 mg・L-1葡萄糖, 温度为10~12℃时, 反硝化途径的氮损提高到30%左右, SAD工艺的平衡受到破坏并向反硝化工艺转变.
S4阶段, 2号反应器出水总氮浓度为4.6~8.0 mg・L-1, 平均值为6.54 mg・L-1, 满足了北京市地方标准的A类排放标准.即使在10~12℃的低温条件下, 氨氮去除率仍保持在90%, 厌氧氨氧化途径的氮损约占85%, SAD工艺运行稳定.以丙酸钠作为碳源时, 低温对SAD工艺的冲击较小.研究表明, 厌氧氨氧化菌可以利用丙酸钠等挥发性脂肪酸, 将硝酸盐还原为氨氮, 且利用挥发性脂肪酸速率大于反硝化细菌[25~27].丙酸钠为基质有利于厌氧氨氧化菌同反硝化菌竞争, 即使在低温条件下, SAD工艺仍能保持高效稳定运行.
2.3 生物学特性研究
为了宏观对比1号和2号反应器中微生物的活性, 定期取滤料进行分析.每次取等量距底部10、30和50 cm的滤料, 测定滤料表面平均生物膜厚度以及污泥反应速率, 结果如图 6所示.
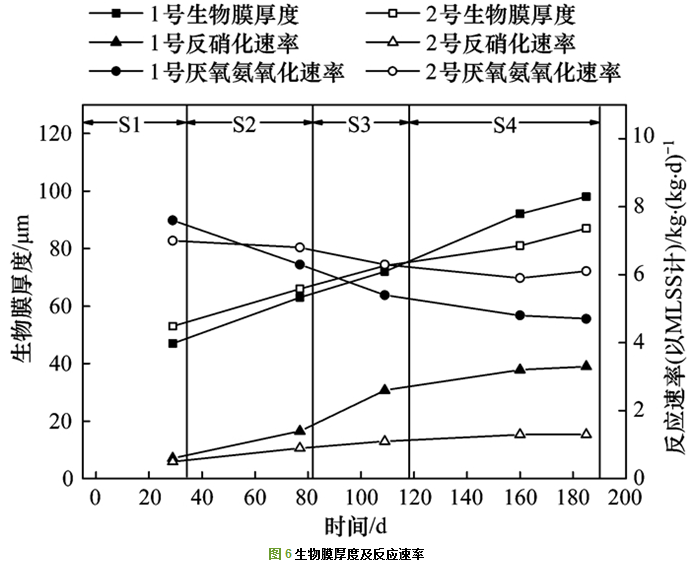
S1阶段1号和2号反应器污泥厌氧氨氧化速率(以MLSS计)分别为7.6 kg・(kg・d)-1和7.0 kg・(kg・d)-1, 两者厌氧氨氧化速率大致相同, 均处于较高水平. S1由于A/O除磷出水中可降解有机物较少, 不利于异养菌的生长, 污泥厌氧氨氧化速率较高, 反硝化速率较低. S2~S4阶段, 基质中投加有机碳源, 有利于反硝化菌的生长, 污泥反硝化速率有所提高.反硝化菌大量增殖, 厌氧氨氧化菌在生物膜中的相对比例有所下降, 因此厌氧氨氧化速率逐步降低.投加有机物的浓度对污泥反应速率影响较大, 随着有机物浓度的升高, 污泥厌氧氨氧化速率逐步下降, 反硝化速率逐渐升高. 1号反应器污泥厌氧氨氧化速率明显下降, 反硝化速率显著增高, 2号反应器污泥反硝化速率增幅较小, 表明碳源种类对污泥反应速率有较大影响.
在反应器运行过程中, 生物膜厚度不断增加. 1号反应器生物膜厚度增长较快, 污泥厌氧氨氧化速率下降明显, 反硝化速率显著升高, 生物膜厚度的增长主要来源于反硝化菌的大量繁殖. 2号反应器生物膜厚度增长较慢, 厌氧氨氧化反应速率和反硝化速率变化幅度较小, 表明适量投加丙酸钠不会导致反硝化菌大量增殖, 2号反应器总氮去除率的提高主要来自厌氧氨氧化菌等微生物的异养代谢.
宏观上, S2~S3阶段, 1号和2号反应器出水总氮浓度, 特征比及亚硝氮氨氮消耗比相差不大, 但污泥反应速率存在较大差距. 1号反应器投加葡萄糖后, 反硝化作用大大增强.反硝化菌将硝氮和亚硝氮转化成氮气, 因此导致亚硝氮氨氮消耗比和特征比的升高.而2号反应器投加丙酸钠, 厌氧氨氧化菌利用丙酸钠将硝氮还原为氨氮, 去除硝氮的同时减少了氨氮消耗, 亚硝氮氨氮消耗比和特征比得以提升.
在市政污水处理厂SAD工艺运行过程中, 应根据温度选择投加碳源的种类和浓度.水温在12℃以上时, 可以投加30 mg・L-1葡萄糖以降低出水总氮浓度; 当水温降低至12℃以下时, 应酌量减少葡萄糖的投加量, 避免SAD工艺向反硝化工艺转变.投加丙酸钠, SAD工艺在10~22℃的环境中均能高效稳定运行.
3 结论
(1) 常温条件(13℃以上)下, 进水投加30 mg・L-1葡萄糖, SAD工艺耦合效果良好, 平均出水总氮浓度为6.41 mg・L-1.相较于厌氧氨氧化工艺, SAD工艺出水总氮浓度降低了42%.低温环境(10~13℃)中, 投加30 mg・L-1葡萄糖, SAD工艺稳定性受到破坏并向反硝化工艺转变.
(2) 常低温环境(10~22℃)中, 基质中投加30 mg・L-1丙酸钠, SAD工艺均有良好的处理效果, 平均出水总氮浓度为6.54 mg・L-1, 丙酸钠对低温SAD工艺影响较小.具体联系污水宝或参见http://www.dowater.com更多相关技术文档。
(3) 投加葡萄糖后, 污泥反硝化速率大大提高.投加丙酸钠后, 污泥反硝化速率增幅较小, 总氮去除率的提高主要来自污泥中细菌异养代谢.建议污水处理厂实际应用中采用丙酸钠作为碳源, 以维持SAD工艺冬季高效稳定运行.