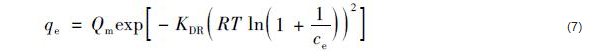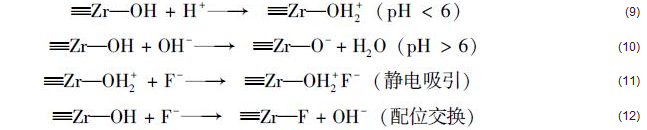氟是人体所必需的重要元素之一, 但是长期饮用氟超标的水可能会引起氟斑牙、氟骨病等疾病.为保证人类健康, 世界卫生组织(WHO)规定饮用水中氟的浓度应低于1.5 mg ・L-1.由于工业排放和含氟矿物的风化淋滤, 世界各地高氟地下水分布范围越来越广, 为人们提供氟未超标的安全饮用水变得尤为重要.目前去除水中氟离子的方法主要有化学沉淀、离子交换、吸附、电渗析和反渗透.与其他方法相比, 吸附法具有经济实用、易于操作、少污染或无污染的特点, 近年来有许多吸附剂运用于水中氟离子的吸附去除, 如活性氧化铝、羟基磷灰石、碳材料、金属氧化物纳米材料等.
锆氧化物纳米材料具有良好的生物相容性、稳定性和低溶解度, 根据HSAB理论(hard-soft-acid-base), 锆与氟之间存在着很强的亲和力, 所以锆氧化物纳米材料具有用作饮用水中氟离子吸附剂的潜力.目前已有大量研究表明锆氧化物纳米材料对溶液中氟离子有良好的吸附性能, 然而纳米材料本身具有较高的表面自由能, 容易团聚而使表面活性位点减少, 从而制约其吸附性能, 并且纳米材料平均颗粒尺寸小, 在处理完含氟水后难以分离和回收, 存在造成二次污染的可能.
石墨烯是一种由碳原子通过sp2杂化而形成的正六边形结构平面薄膜, 只有一个原子厚度的新型二维碳材料.石墨烯拥有极大的比表面积和丰富的表面官能团, 对染料和金属离子有优异的吸附性能, 尽管已有研究称石墨烯可用作氟离子吸附剂, 但石墨烯和氟离子间微弱的相互作用力降低了其吸附能力.石墨烯大比表面的特点使其成为多种纳米材料的良好载体, 与其它纳米材料复合可实现优势互补的目的.
本研究结合锆氧化物对氟较强亲和力和石墨烯大比表面积的优点, 通过均相沉淀法将水合氧化锆(HZO)非晶薄层均匀涂盖在三维网状结构的石墨烯水凝胶(SGH)表面, 成功制备出HZO@SGH. HZO@SGH保持了石墨烯大比表面积的特点, 同时防止HZO团聚现象的产生, 从而避免HZO表面活性位点减少, 使得HZO@SGH的吸附性能得到明显提升.三维网状结构HZO@SGH通过重力作用能很快沉降到溶液底部, 易于分离和回收.本实验采用HZO@SGH作为吸附剂, 去除模拟含氟水中的氟离子, 系统地研究HZO@SGH吸附氟离子的吸附动力学和静态吸附等温线, 探究了溶液初始pH和共存离子对HZO@SGH吸附性能的影响, 分析了HZO@SGH吸附氟离子的机制.
1 材料与方法 1.1 药品与试剂
天然石墨粉(325目)、水合氯氧化锆(ZrOCl2 ・8H2O)、氟化钠(NaF)购自上海阿拉丁生化科技股份有限公司; 其他试剂均为分析纯; 实验用水为纯水.
1.2 吸附剂的制备
氧化石墨烯(GO)通过经典的Hummers法制备.石墨烯水凝胶(SGH)通过将30 mg抗坏血酸钠充分溶解到2 mg ・L-1的GO分散液中, 90℃水浴条件下加热90 min制备.
HZO@SGH通过将SGH置于氯氧化锆(0.3mol ・L-1)和尿素(1.8mol ・L-1)的混合液中浸渍24 h, 之后在95℃水浴条件下加热90 min制备.
1.3 实验方法
动态吸附实验:取已知浓度的氟离子溶液于500 mL塑料大口瓶中, 加入0.3g ・L-1HZO@SGH吸附剂后置于25℃条件下的恒温水浴摇床中振荡, 每隔预定时间取样.
静态吸附实验如下.
(1) 吸附等温线研究 取20 mL预先配置的浓度为2~20 mg ・L-1的氟离子溶液于50 mL塑料大口瓶中, 加入0.3 g ・L-1的HZO@SGH吸附剂后置于25℃条件下的恒温水浴摇床中振荡5 h取样.
(2) 初始pH值影响 取20 mL初始浓度为5 mg ・L-1的氟离子溶液于50 mL塑料大口瓶中, 加入0.3g ・L-1的HZO@SGH吸附剂并用0.1 mol ・L-1的NaOH或HCl调节溶液pH值至3~10, 置于2℃条件下的恒温水浴摇床中振荡5 h取样.
(3) 共存阴离子影响 批量将0.3g ・L-1的HZO@SGH投加到20 mL含有5 mg ・L-1氟离子及不同浓度的单一阴离子溶液中, 在25℃水浴摇床中振荡5 h取样.
所有批次实验采用离子色谱法测定溶液剩余氟离子浓度, 氟离子的吸附量由式(1)计算:
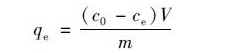 (1)
(1)
式中, c0(mg ・L-1)表示初始氟离子浓度, ce(mg ・L-1)表示剩余氟离子浓度, V(mL)表示氟离子溶液体积, m(mg)表示投加的吸附剂质量, qe(mg ・g-1)表示氟离子的吸附量.
2 结果与讨论 2.1 材料表征 2.1.1 XRD表征
图 1是GO、SGH、HZO和HZO@SGH的XRD表征图.从中可看出, GO在2θ=10.4°处有一尖锐的衍射峰, 经计算其层间距大约为0.85 nm, 明显高于天然石墨(0.34 nm), 这是由于在GO的制备过程中大量含氧官能团的引入, 改变了石墨的固有结构, 使得层间距明显增加. SGH在2θ=23.5°处有一较宽的衍射峰, 经计算其层间距大约为0.38 nm, 明显低于GO但略微高于天然石墨, 表明在SGH中存在着石墨烯片层间的π-π堆垛且SGH仍然残留有部分的含氧官能团.在HZO和HZO@SGH的XRD图谱中未发现明显的衍射峰, 表明HZO属于无定形的物质, 且在HZO@SGH复合物中, HZO完全覆盖于SGH表面.
2.1.2 SEM表征
图 2(a)和2(b)是石墨烯水凝胶的SEM图, 从中可观察到石墨烯水凝胶是由二维结构石墨烯片层组成, 具有特殊的三维网状结构.通常, HZO可通过向氯氧化锆溶液中滴加NaOH促进氯氧化锆水解制备, 这种方法反应太过迅速难以控制, 本研究所采用的均相沉淀法反应缓慢, 可通过控制反应温度和时间来控制尿素的分解速度, 从而控制氯氧化锆的水解速度, 使得生成的HZO能够均匀地包覆到SGH的表面.图 2(c)和2(d)是HZO@SGH复合吸附剂的SEM, 从中可看出HZO@SGH的结构是连续均一的, 即使在局部放大的图 2(d)中也未发现颗粒结构的存在, 并且HZO@SGH仍具有和SGH类似的形貌结构, 这表明在制备HZO@SGH的过程中, SGH的三维网状结构并未被破坏.
2.1.3 红外光谱图分析
样品表面的各类官能团可通过傅里叶变换红外光谱(FTIR)分析.图 3为GO和吸附氟离子前后的HZO@SGH的红外光谱图, 从中可知, 3个样品在3 456 cm-1处都出现了一个较宽的吸收峰, 这是样品表面吸附水的―OH的伸缩振动峰.在GO的红外光谱图中, 1 730 cm-1和1 416 cm-1处的吸收峰是羧基(C=O和O―C=O)的伸缩振动, 1 226 cm-1处的吸收峰是环氧基(C―O―C)的伸缩振动峰, 1 628 cm-1处的吸收峰是GO的C―C骨架振动峰和其表面水O―H的弯曲振动峰, 1 065 cm-1处的吸收峰是烷氧基(C―O)的伸缩振动峰.在HZO@SGH的红外光谱图中, 都存在1 643 cm-1处的特征峰, 这是吸附剂表面吸附水O―H的弯曲振动峰, 此外, 在吸附前的HZO@SGH红外光谱图中有1 563 cm-1和1 358 cm-1处的特征峰, 对应Zr―OH的振动峰, 而在吸附后的HZO@SGH红外光谱图中, 两处的特征峰都已消失, 这表明吸附剂表面的羟基基团在吸附过程中被氟离子取代而大量减少.
2.1.4 XPS表征
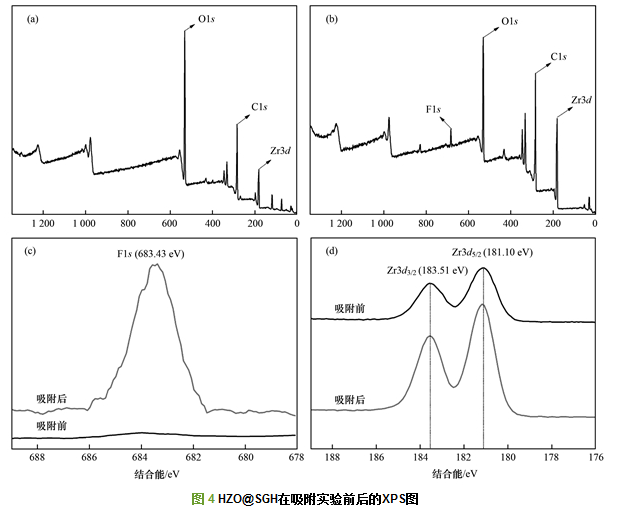
XPS表征可用来探究HZO@SGH吸附剂表面元素组成在吸附实验前后的变化, 表征结果如图 4所示.比较图 4(a)和4(b)可发现HZO@SGH未吸附氟离子之前的全谱图未发现F1s峰, 而HZO@SGH吸附氟离子后出现了一个较强的F1s峰, 这说明了HZO@SGH能够成功吸附溶液中的氟离子, 图 4(d)氟的XPS分谱图中F1s的结合能在吸附实验前后的改变也证实了这点.溶液中氟离子在HZO@SGH上的吸附机制可大致由图 4(c)解释, 在吸附实验前, 锆的XPS分谱图在181.10 eV和183.51 eV处出现了两个峰, 分别对应于Zr3d5/2和Zr3d3/2, 而在吸附氟离子之后, Zr3d5/2和Zr3d3/2都向左发生了0.21 eV和0.13 eV的化学位移, 这是由于吸附剂表面的锆与溶液中电负性更强的氟离子相结合而形成氟化锆或锆的氟氧化物, 使得锆的电负性增强, 导致其外层电子密度减小, 对内层电子的屏蔽作用相应减弱, 因此锆的内层电子结合能增加, 所以Zr3d5/2和Zr3d3/2发生了化学位移.
2.2 批次吸附实验 2.2.1 不同吸附剂吸附性能比较
在25℃, pH=6.5, 氟离子初始浓度为5 mg ・L-1的条件下, HZO、SGH和HZO@SGH去除溶液中氟离子的吸附性能如图 5所示, HZO虽然与溶液中氟离子有很强的亲和力, 但团聚现象的产生减少了其表面活性位点, 降低了其吸附性能, 饱和吸附量为5.57mg ・g-1. SGH表面含有少量与溶液中氟离子相排斥的电负性含氧基团, 降低了其吸附性能, 饱和吸附量仅为1.83mg ・g-1.相反, 由于HZO@SGH复合吸附剂能够避免HZO的团聚, 同时保持了SGH大比表面积的特点, 使得HZO@SGH的吸附性能得到显著提升, 饱和吸附量达到15.92 mg ・g-1.此外, 在氟离子溶液中三维网状HZO@SGH比HZO纳米颗粒有更好的可分离性, 如图 6所示, 经过1 h静置, HZO@SGH通过重力作用已完全沉降到溶液底部, 而HZO纳米颗粒仍有部分悬浮在溶液中.优异的可分离性使得HZO@SGH在处理完含氟水后能够很好地从溶液中分离出来, 避免造成二次污染的可能.
2.2.2 吸附动力学研究
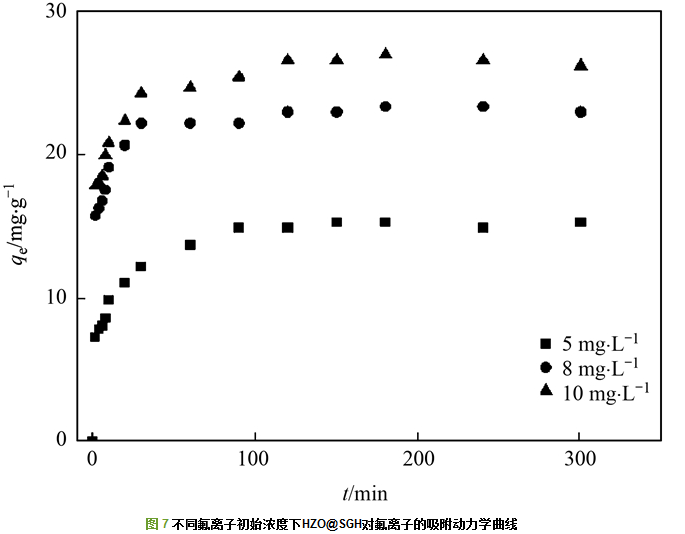
吸附动力学研究是一种探究吸附过程的重要方法.在25℃, pH=6.5, 不同氟离子初始浓度(5、8和10 mg ・L-1)条件下, HZO@SGH去除氟离子的吸附动力学曲线如图 7所示, HZO@SGH对氟离子的吸附量随着溶液中氟离子初始浓度增加而增大, 在吸附前30 min, 吸附速率较快, 随后吸附速率逐渐减小, 在300 min基本达到吸附平衡.
为进一步探究HZO@SGH去除溶液中氟离子的吸附动力学过程, 本研究采用拟一级和拟二级动力学模型对吸附动力学实验数据进行拟合分析.两个动力学模型可分别由以下方程式表示:
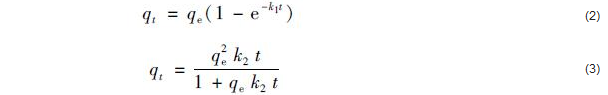
式中, t(min)为吸附质与吸附剂的接触时间; qt(mg ・g-1)为t时刻的吸附量; qe(mg ・g-1)表示平衡吸附量; k1 (min-1)为拟一级动力学常数; k2 [g ・(mg ・min)-1]为拟二级动力学常数.
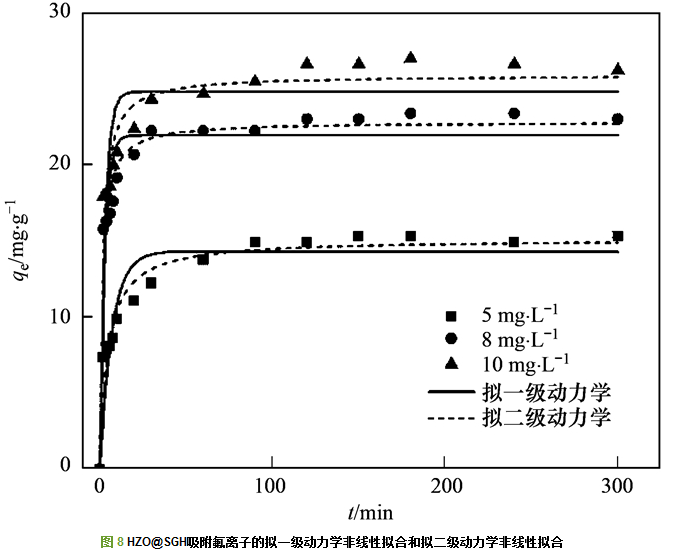
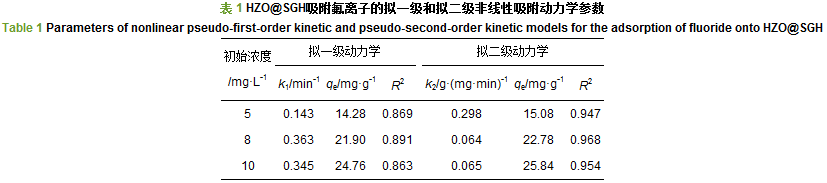
利用拟一级动力学方程和拟二级动力学方程对HZO@SGH吸附氟离子进行拟合, 拟合结果如图 8所示, 拟合参数见表 1.从中可看出, 拟二级动力学相关系数(R2>0.968)均高于拟一级动力学相关系数, 表明氟离子在HZO@SGH上的吸附动力学更符合拟二级动力学模型, 这说明吸附速率主要是由HZO@SGH与氟离子间的配位交换和静电吸引相关的化学吸附控制.
2.2.3 等温线研究
本文通过等温线模型来探究HZO@SGH对氟离子的吸附机制, 选择Langmuir、Freundlich和Dubinin-Radushkevich这3种等温模型进行拟合
Langmuir等温模型假设吸附剂表面性质均一, 吸附质分子在吸附剂表面为单层吸附且吸附质分子间无作用力.非线性Langmuir吸附等温模型可由式(4)表示:
式中, qe(mg ・g-1)为平衡吸附量; qmax(mg ・g-1)为最大吸附量; ce(mg ・L-1)为剩余氟离子浓度; KL(L ・mg-1)为Langmuir吸附等温式常数.
吸附过程的性质可根据一种无量纲常数即分离系数RL判断, RL可由式(5)表示:
式中, c0(mg ・L-1)为初始氟离子浓度.当RL>1时表示非优惠吸附; 0 < RL < 1表示优惠吸附; RL=0表示不可逆吸附; RL=1表示线性吸附.
Freundlich吸附等温方程是一种基于假设吸附剂表面是非均一的经验方程, 其非线性形式可由式(6)表示:
式中, KF[(mg ・g-1) ・(L ・mg-1)]为Freundlich吸附等温式常数; 1/n为一种反映吸附强度的无量纲常量.
Dubinin-Radushkevich等温模型常用于描述多孔材料的吸附过程和机制, 可由式(7)表示:
式中, Qm(mg ・g-1)为理论饱和吸附量, KDR(mol2 ・kJ-2)为Dubinin-Radushkevich吸附等温式常数.吸附自由能E(kJ ・mol-1)常用于判断吸附质在吸附剂表面的吸附机制, 可由式(8)表示:
当E的值介于8~16 kJ ・mol-1, 说明吸附质主要通过化学吸附作用吸附到吸附剂表面.
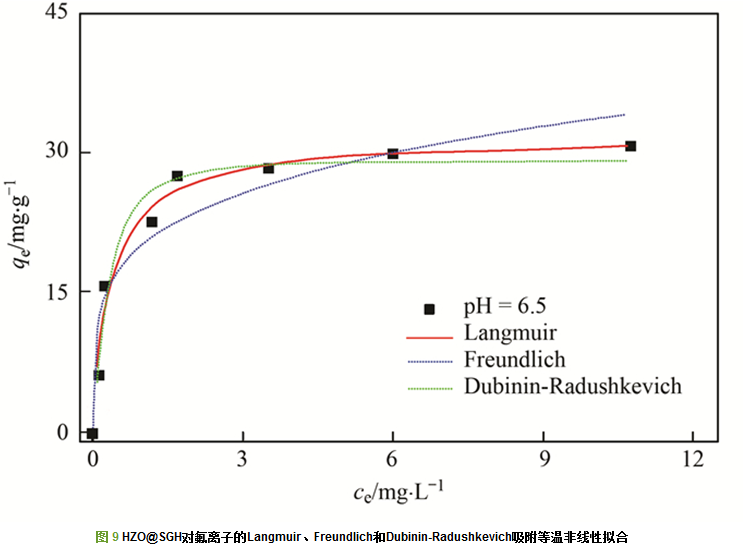
在常规条件下(25℃, pH=6.5), 测定HZO@SGH对不同初始浓度氟离子的吸附量, 并用Langmuir、Freundlich和Dubinin-Radushkevich吸附等温模型进行非线性拟合, 拟合结果如图 9所示, 拟合参数见表 2.从中可看出, Langmuir等温模型R2=0.955, Freundlich等温模型R2=0.891, Dubinin-Radushkevich等温模型R2=0.974, 比较各模型相关系数R2大小可知HZO@SGH对氟离子的吸附过程更符合Dubinin-Radushkevich等温模型.在氟离子溶液初始pH=6.5条件下, 根据式(5)估算的RL=0.018, 说明氟离子在HZO@SGH的吸附类型是优惠吸附; 根据式(8)估算的E=9.87 kJ ・mol-1, 说明溶液中氟离子主要通过静电吸引和配位交换等化学吸附作用吸附到HZO@SGH表面.根据图 9还可知, HZO@SGH达到吸附平衡后, 溶液中氟离子浓度从初始的≤8 mg ・L-1减小到≤1.19 mg ・L-1, 低于WHO规定的饮用水中氟离子的标准浓度(1.5 mg ・L-1), 表明HZO@SGH具有吸附去除饮用水中氟离子的应用潜力.
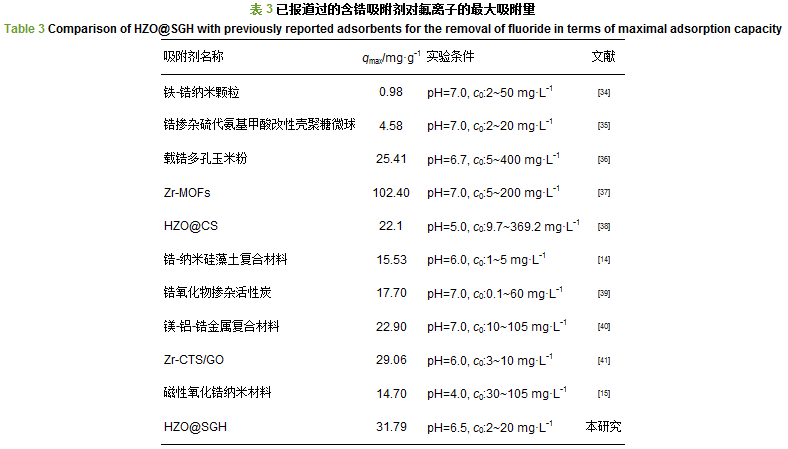
表 3为前人所报道过的含锆复合吸附剂和本研究所制备的HZO@SGH对溶液中氟离子最大吸附量的对比.本研究通过可控的均相沉淀法制备的HZO@SGH, 能够使HZO均匀地涂盖到SGH表面, 既避免了HZO团聚的产生而使其活性位点减少, 又保持了石墨烯大比表面积的特点, 所以由表 3可看出本研究所制备的HZO@SGH较部分含锆复合吸附剂有更优异的吸附性能.
2.2.4 初始pH值影响
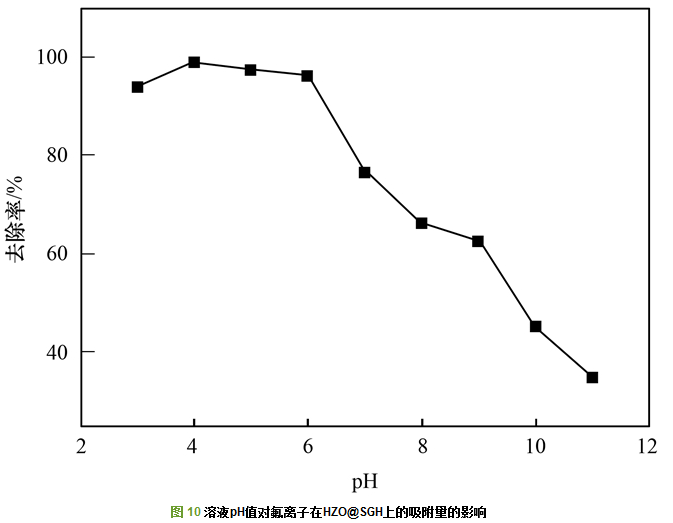
氟离子溶液的pH值大小是影响吸附剂吸附性能的重要因素之一.根据图 10分析可知, 在pH为3~6.5的范围内, HZO@SGH对氟离子的去除率达到89%以上, 当溶液pH为4时, 氟离子的去除率达到最大值98%.随着溶液pH值从6减小到4, HZO@SGH对溶液中氟离子的去除率略微增大, 这是因为在pH值较低的环境下, 大量的H+使得吸附剂表面质子化而产生更多带正电的吸附位点, 增强了其与电负性氟离子的静电作用, 使更多的氟离子被吸附到吸附剂表面, 如化学方程式(9)和(11)所示.而当溶液pH值从4减小到3或是从6增大到11, HZO@SGH的吸附性能都呈现下降趋势, 前者可能是由于在更低的pH值条件下, 溶液中形成了HF而使能够吸附到HZO@SGH上的游离的氟离子减少, 后者则是因为随着溶液pH值的上升, HZO@SGH表面的质子化作用逐渐减弱且溶液中大量OH-的存在会与氟离子竞争吸附剂表面的吸附位点, 从而导致氟离子在吸附剂上的吸附量减少, 并且在较高的pH条件下, 氟离子吸附到HZO@SGH主要是通过配位交换实现的, 如化学方程式(10)和(12)所示.
2.2.5 共存离子影响
在实际的含氟地下水中除了含有氟离子外可能还存在其他阴离子, 多种阴离子的共存可能会与氟离子一起竞争吸附剂表面的吸附位点而导致吸附剂对氟离子的吸附量的减少.为了探讨HZO@SGH在含有不同浓度阴离子的含氟水中的吸附性能, 在25℃, pH=6.5的条件下, 本实验设置NO3-、Cl-、SO42-、CO32-和PO43-这5种常见阴离子作为共存离子, 研究共存离子对氟离子在吸附剂上的吸附量的影响, 其结果如图 11所示.
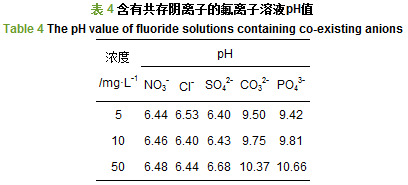
根据图 11分析可知, 含氟水溶液中NO3-、Cl-浓度的增加对氟离子在HZO@SGH上的吸附量几乎没有影响, SO42-在浓度小于10 mg ・L-1时, 其对HZO@SGH吸附性能的影响较小, 但是CO32-和PO43-浓度的增加却导致氟离子在HZO@SGH上的吸附量显著下降.这其中存在着两方面的原因:一是由于阴离子的表面电荷密度越大, 其与吸附剂的亲和力越强, 而多价态离子的表面电荷密度一般都大于单价离子, 所以溶液中NO3-和Cl-的存在对影响吸附剂吸附氟离子的性能比SO42-、CO32-和PO43-小;二是因为其他阴离子的存在可能会改变溶液的pH值, 从表 4可看出, CO32-和PO43-在溶液中大量存在会因其发生水解而产生大量OH-使溶液碱性增强, 使得氟离子在吸附剂上的吸附量减小.
3 结论
(1) 采用均相沉淀法制备HZO@SGH吸附剂, 通过XRD和SEM表征手段可知HZO属于无定形结构, 能够均匀地涂盖到SGH表面使得HZO@SGH保持SGH独特的三维网状结构.
(2) HZO@SGH对氟离子的吸附容量明显高于HZO和SGH. HZO@SGH在氟离子溶液中的可分离性优于HZO, 通过静置1h后可完全沉降到溶液底部, 便于分离回收, 防止二次污染的可能.
(3) 氟离子在HZO@SGH上的吸附动力学符合Lagergren拟二级动力学方程, 说明吸附速率主要由化学吸附控制.吸附过程可由Dubinin-Radushkevich吸附等温模型描述, 吸附自由能E=9.87 kJ ・mol-1, 说明溶液中氟离子主要通过化学吸附作用吸附到HZO@SGH表面.吸附剂最大吸附量可达31.79mg ・g-1, 优于部分已报道的含锆复合吸附剂.
(4) HZO@SGH在较宽的pH值(pH为3~6.5)范围内对溶液中氟离子的去除率能够保持89%以上, 在pH为4的条件下达到最大去除率98%;含氟水溶液中存在NO3-或Cl-对HZO@SGH的吸附性能几乎没有影响, 存在较低浓度的SO42-(≤10 mg ・L-1)时, HZO@SGH的吸附性能略微减小, 而当溶液中存在CO32-或PO43-时, 氟离子在HZO@SGH上的吸附量随着两种离子浓度的增加而急剧下降.具体联系污水宝或参见http://www.dowater.com更多相关技术文档。
(5) 通过红外光谱、XPS表征和初始pH影响实验分析可知氟离子吸附在HZO@SGH上的吸附机制主要是氟离子与质子化的吸附剂间的静电引力作用和氟离子与吸附剂表面羟基间的配位交换作用.