磷是水生植物生长所必需的营养元素。近年来,随着水体中营养盐含量持续升高,出现了藻类繁殖,水体中溶解氧显著下降,水中生物多样性锐减,甚至生态系统崩塌等一系列环境问题。磷进入水环境的主要途径是含磷工业废水、生活污水的排放,以及磷肥、畜禽粪便等经过雨水淋洗随地表径流进入水体。因此,在污水排放前有效去除磷,是控制水体富营养化的重要手段。目前,常用的除磷方法主要有化学沉淀法、生物法、反渗透法、离子交换与吸附法等。其中,吸附法具有吸附量大、操作简单、污泥产量少以及成本低等优点,并且还可作为其他除磷方法的补充,。因此,探寻高效且成本低廉的磷吸附新型材料成为环境领域研究的热点。
类水滑石化合物(layered double hydroxides,LDHs),也称为层状双金属氢氧化合物,其化学组成通式为[M2+1−xM3+x(OH)2][An−x/n・mH2O],其中M2+、M3+分别代表二价和三价金属阳离子,x指金属元素的含量变化,范围在0.2~0.33之间,An−代表层间可交换阴离子。其合成方法简单方便,且成本较低。良好的阴离子交换性能使其成为去除水体阴离子污染物的优良吸附材料。关于Mg-Al和Zn-Al LDHs等对于磷酸根的吸附已有报道,但吸附容量有待提高。原因在于,水滑石层板主体和层间强烈的静电引力使得内表面具有部分不可到达性,且天然形成的镁铝水滑石层间阴离子为碳酸根,相比磷酸根,碳酸根与层板的亲附力更强,一定程度上限制了其对磷酸根的离子交换能力。
通过剥层水滑石获得纳米片具有广泛的应用前景,水滑石纳米片层带正电荷,具有分子水平的二维尺度,可作为基础材料与阴离子型聚合物制备多层超薄复合膜材料,也可通过层层自组装制备石墨烯氧化物复合材料,以及将其作为药物载体,电磁材料等。水滑石纳米片具有尺寸小、比表面积大、活性位暴露程度高等优点,相比于传统的水滑石具有更好的吸附潜力。
LDHs层片带高密度的正电荷,与层间阴离子存在较强的静电作用,因而其剥离难度较大。ADACHIPAGANO等于2000年报道了表面活性剂十二烷基硫酸钠(SDS)插层的Zn2Al-Cl LDHs在丁醇中的剥离。将Zn2Al-SDS LDHs置于丁醇中在120 °C条件下回流12 h,得到透明的分散体系,表明LDHs被剥离。HU等提出利用反相微乳液法在十二烷基硫酸钠-水-异辛烷中可直接制备固态的LDHs纳米片。利用异辛烷作为助表面活性剂,将镁铝混合盐溶液与硝酸钠和氢氧化钠混合碱溶液分散于十二烷基硫酸钠/丁醇混合体系中,于75 °C下搅拌24 h后离心、洗涤,得到横向尺寸为40~50 nm、厚度约为10 nm的LDHs。通过上述方法获得水滑石纳米片层的过程比较复杂且耗时较长。YU等采用一步法直接在甲酰胺合成水滑石纳米片结构,与剥离法不同,该法是在合成过程中引入层生长抑制剂――甲酰胺,它的羰基和水滑石中的羟基结合形成氢键,代替了原本层间的水分子,而甲酰胺中的氨基与层间的阴离子作用很弱,这样减弱了层间的静电引力,只允许层板横向生长,抑制其在z方向上的生长,从而形成单层的片状结构。这种方法提供了一种新的途径,并且可能制备出更多有价值的材料。
本研究通过调控镁铝反应物浓度,结合XRD、SEM和TEM等手段对一步法在甲酰胺中制备水滑石纳米片的方法进行了优化;通过吸附热力学、动力学实验对该材料对磷酸盐的吸附性能进行了分析;通过Zeta 电位、XPS 等方法对磷酸根在水滑石纳米片表面的吸附行为和机理进行了解析。
1 实验部分
1.1 实验材料
本研究中用到的六水合硝酸镁、九水合硝酸铝、甲酰胺、磷酸二氢钾、硝酸钠、氢氧化钠(98%)、浓硝酸(68%)、浓硫酸(98%)、酒石酸锑氧钾、钼酸铵、抗坏血酸等试剂来自于国药集团化学试剂有限公司,均为分析纯。
1.2 水滑石纳米片的制备
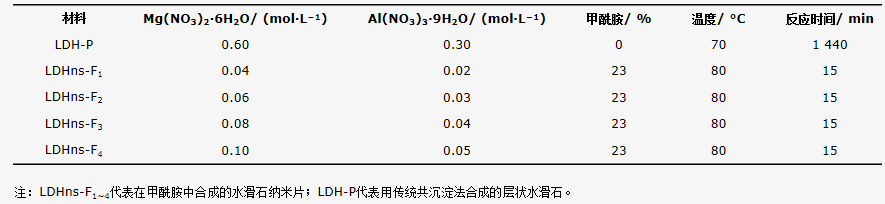
将100 mL含有质量分数23%的甲酰胺和0.01 mol・L−1NaNO3的溶液置于80 °C水浴锅中。将不同浓度(见表1)、镁铝摩尔比为2:1的Mg(NO3)2・6H2O和Al(NO3)3・9H2O混合均匀溶于200 mL去离子水。向甲酰胺溶液中同时逐滴滴加镁铝混合溶液和0.5 mol・L−1NaOH,控制反应体系pH为10。在高纯氮气保护下,磁力搅拌15 min,而后在10 000 r・min−1下高速离心,用乙醇和脱CO2的去离子水反复离心洗涤3遍,于冷冻干燥机中干燥24 h后,研磨得到水滑石纳米片粉末(LDHns-F1~4)。
表1 层状水滑石和水滑石纳米片的合成溶液组成、温度及反应时间
作为对比,按照传统的共沉淀方法合成层状水滑石(LDH-P)。在室温条件下,按照镁铝摩尔比2:1准确称量一定质量的Mg(NO3)2・6H2O和Al(NO3)3・9H2O,溶于盛有200 mL去离子水的锥形瓶中,70 °C水浴搅拌至完全溶解。期间通入氮气,驱赶溶液中的CO2。待盐溶解后,逐滴加入0.5 mol・L−1NaOH使之发生沉淀反应,至溶液pH为9。pH恒定后停止搅拌。陈化24 h后,用去离子水反复离心洗涤。将所得膏体冷冻干燥,研磨后即为水滑石吸附剂LDH-P。材料合成条件见表1。
1.3 等温吸附实验
(25±1) °C下,在50 mL离心管中,准确加入0.03 g的吸附剂、一定量的去离子水和NaNO3,使其离子强度为0.01 mol・L−1,将悬浊液置于超声波浴(80 kHz)30 min。然后向离心管中加入不同体积的KH2PO4工作液,使磷浓度为10~120 mg・L−1,总体积为30 mL。用0.1 mol・L−1 HNO3和NaOH调节溶液pH为8.5±0.1。在恒温振荡箱(170 r・min−1)中振荡24 h。振荡过程中,每隔5 h重新调节溶液的pH使其保持恒定。反应结束后离心,上清液用0.22 μm的微孔滤膜过滤后采用紫外可见分光光度计(UV-756 PC,上海恒平公司)测定磷浓度。
1.4 吸附动力学实验
(25±1) °C下,在50 mL离心管中,准确加入0.03 g的吸附剂、一定量的去离子水和NaNO3,使其离子强度为0.01 mol・L−1,将悬浊液置于超声波浴(80 kHz)30 min。随后,分别向离心管中加入磷初始浓度为80、100、150 mg・L−1的磷酸盐溶液,使其总体积为30 mL。用0.1 mol・L−1 HNO3和NaOH调节溶液pH为8.5±0.1,在170 r・min−1下磁力搅拌。每隔一定时间取出离心管,在10 000 r・min−1下离心分离5 min,用0.22 μm的微孔滤膜过滤,取上清液,测定磷浓度。
1.5 材料表征与分析方法
X射线衍射(XRD)用于分析样品的晶相,采用X'Pert PRO MPD型X射线衍射仪(PANalytical公司,荷兰)来测定,CuKα射线(λ = 0.154 08 nm,40 kV,40 mA),扫描范围为5°~90°,扫描速度为0.13(°)・s −1。将离心后的膏状湿样涂抹在玻璃样品槽中,并覆盖迈拉膜以减少测定过程中水分蒸发,使膜表面平坦。作为对比,将冷冻干燥的粉末样品同样填充到样品槽中,并用压制法将表面压平,用盖玻片除去多余的粉末后进行测定。
采用场发射扫描电子显微镜(FESEM,HU8020,日本Hitachi公司)观察水滑石纳米片的微观结构及形貌的变化。仪器工作电压为10 kV,测试时,将粉末通过黏附在具有导电性黑色胶带的硅片表面上,喷金处理后进行测试。
使用透射电子显微镜(TEM,H-7500,日本Hitachi公司)观察水滑石纳米片的晶体尺寸及形貌。透射电镜样品制备如下:称取约10 mg样品于200 mL乙醇中,在80 kHz下超声30 min后取一滴上清液置于在铜网的碳膜上,常温下在空气中干燥。
采用X射线光电子能谱(XPS,Quantera II,日本Ulvac-Phi公司)宽谱扫描进行样品表面元素的种类及相对含量的分析,宽谱的采集范围为0~1 400 eV,通过能为280 eV。采用XPS窄谱扫描进行元素的化学态及各种化学态的相对含量分析,C1s和P2p谱的通过能为140 eV,高分辨O1s谱的通过能为26 eV。采用XPSPEAK41软件对氧元素谱图进行分峰拟合。样品处理:在进行XPS分析前进行干燥处理,以避免残留溶剂和水等对仪器分析部件的污染,并缩短抽真空的时间。在导电胶上撒上一层处理好的待测样品,然后抖掉松散样品颗粒,放入分析室进行分析。
采用Zetasizer Nano ZS电位分析仪(英国Malvern Instrument Ltd.公司)测量纳米片在吸附磷前后的Zeta电位。向0.01 mol・L−1的NaNO3溶液中加入0.03 g水滑石纳米片,磷初始浓度为50 mg・L−1,总体积为30 mL。用0.1 mol・L−1NaOH或0.1 mol・L−1HNO3溶液将反应pH调节至4.0、5.0、6.0、7.0、8.0、9.0、10.0、11.0。调节完成后,将悬浊液置于25 °C恒温摇床,170 r・min−1振荡,每隔5 h重新调节pH。24 h后取出并静置30 min,取1 mL悬浮液转移到样品管进行Zeta电位测量。
2 结果与讨论
2.1 镁铝反应物浓度对水滑石纳米片的影响
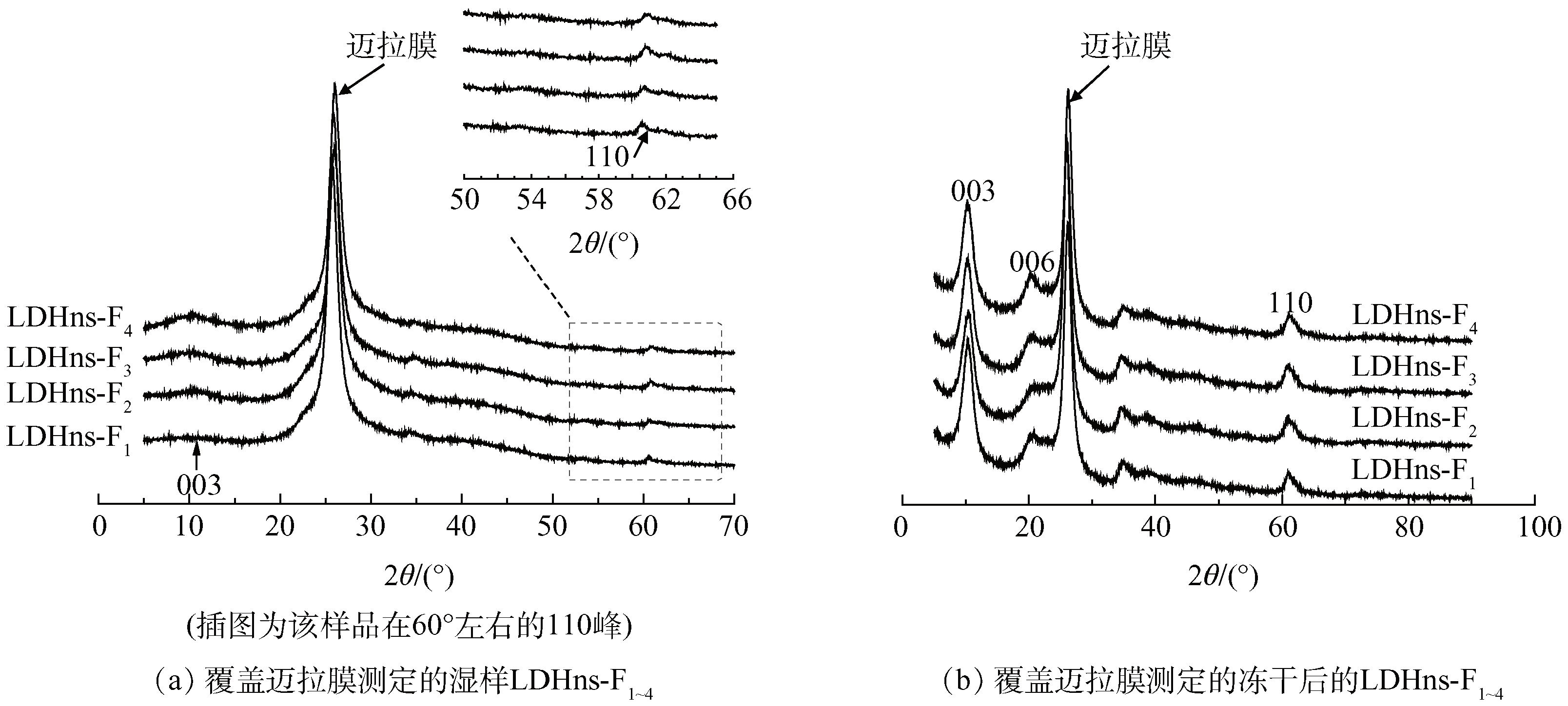
XRD结果显示,将离心后的LDHns-F1~4样品直接在湿润状态下进行XRD测定时,该4个样品都不具备明显的层状水滑石特征峰(003)峰(图1(a)),而经冻干后,4个样品出现了不同强度的(003)峰(图1(b))。(003)峰的缺失表明湿润的LDHns-F1~4样品长程有序性的缺失,层板不再平式堆叠所以不会引起X射线干涉。当样品冻干后,一个宽而强的峰在10.75°(0.82 nm)处出现(图1(b)),这可能是由干燥引起水滑石纳米片堆叠造成的。对照层状水滑石,LDHns-F1~4湿样中(003)峰和(006)峰缺失而(110)峰依然存在,表明LDHns-F1~4纳米片具有水滑石的二维结构特征。这些证据与文献中所报道的剥离后水滑石纳米片的证据,吻合,表明该实验合成的纳米片纵向几乎不堆叠。然而,随着合成镁铝反应物浓度的增加,湿样中(003)峰也逐渐开始显现(图1(a)),说明镁铝浓度升高会一定程度造成纳米片的团聚。
图1 覆盖迈拉膜测定的冻干前后LDHns-F1~4的XRD图谱
水滑石纳米片LDHns-F3的扫描电镜如图2(a)、(b)所示。整体上看,超薄的纳米片是均匀分布的。合成反应时间短(15 min)导致纳米片尺寸较小、薄且卷曲。这些结果也与XRD图谱中相对较低的结晶度一致(图1(b))。扫描电镜显示这些LDH纳米片呈板状形貌和六角形微晶的特点。透射电镜的结果也证实了LDH纳米片超薄的特性。LDHns-F3的横向尺寸约为30 nm(图2(c)插图)。由于超薄的特点,平铺的LDH纳米片在某些区域是非常透明的,甚至光可以透过片层。图2(c)中细长的深色区域,表明一些超薄的纳米板垂直且呈卷曲状。随着镁铝反应物浓度的增加,LDHns-F4的透射电镜图中纳米片发生较多团聚(图2(d)),这与XRD(图1(a))结果中(003)峰的增加相对应。为使纳米片具有较好的分散性,同时考虑到材料中LDHns-F3产量较高,因此,本研究主要以LDHns-F3为研究对象进行分析和吸附机理研究。
图2 LDH纳米片的扫描电镜图和透射电镜图
2.2 水滑石样品的吸附性能
2.2.1 层状水滑石和纳米片的吸附等温线
层状水滑石和纳米片的吸附分别采用Langmuir和Freundlich模型进行拟合。Langmuir模型设定吸附过程是吸附剂均质表面的单层吸附,且吸附质分子之间没有相互作用;Freundlich模型是一个经验方程,通常用于描述异质表面的多层化学吸附。具体联系污水宝或参见http://www.dowater.com更多相关技术文档。
Langmuir吸附等温线模型:
qe = qmaxKLCe/(1+ KLCe) (1)
式中:qe和qmax分别为吸附量和最大吸附量,mg・g−1;KL为Langmuir吸附常数,L・mg−1;Ce为吸附质平衡浓度,mg・L−1。
Freundlich吸附等温线模型:
qe = KFCe1/n(2)
式中:qe为平衡吸附量,mg・g−1;Ce为吸附质平衡浓度,mg・L−1;KF为与吸附有关的常数、n为常数。
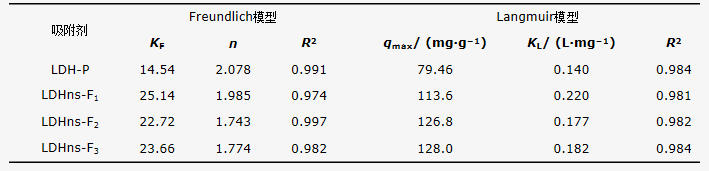
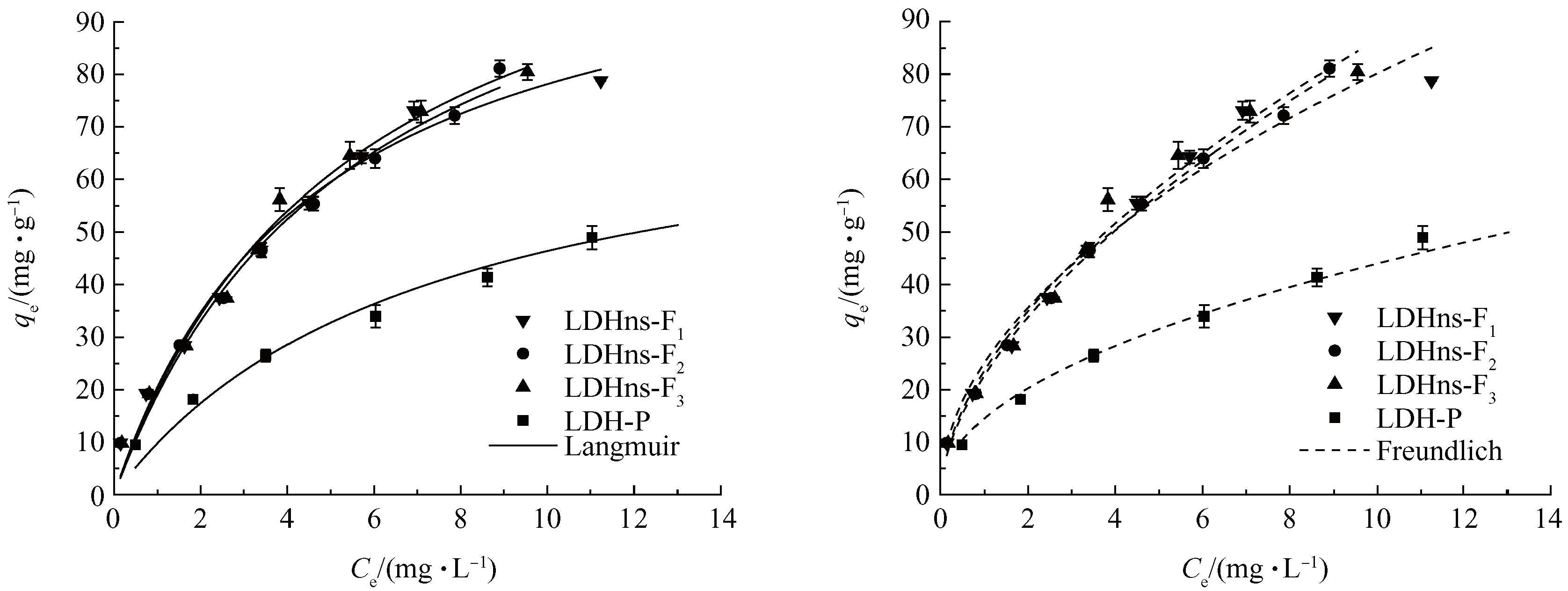
吸附等温线拟合相关系数如表2所示,R2均在0.97以上,表明吸附实验数据的拟合度较好,层状水滑石和纳米片对磷酸盐的吸附效果介于2种吸附模型之间,说明吸附剂对吸附质的吸附不仅是单分子层的吸附,吸附过程较为复杂。从Langmuir模型中拟合出LDHns-F1、LDHns-F2、LDHns-F3的最大吸附量分别为113.6、126.8、128.0 mg・g−1,而层状水滑石LDH-P的最大吸附量仅为79.46 mg・g−1。从吸附等温线(图3)可以看到,所有的水滑石纳米片对于磷酸根的吸附量均高于层状的水滑石结构。不同镁铝反应物浓度合成的水滑石纳米片吸附量相近。但是,本研究中LDHns-F3与YU等[26]报道的合成方法相比,产量提高了50倍(达到1.6 g),大大提高了吸附剂的合成效率并节约了成本。
表2 层状LDH和纳米片的Freundlich和Langmuir模型拟合参数
图3 LDH-P和LDH纳米片的吸附等温线及Langmuir和Freundlich模型拟合
2.2.2 水滑石纳米片的吸附动力学
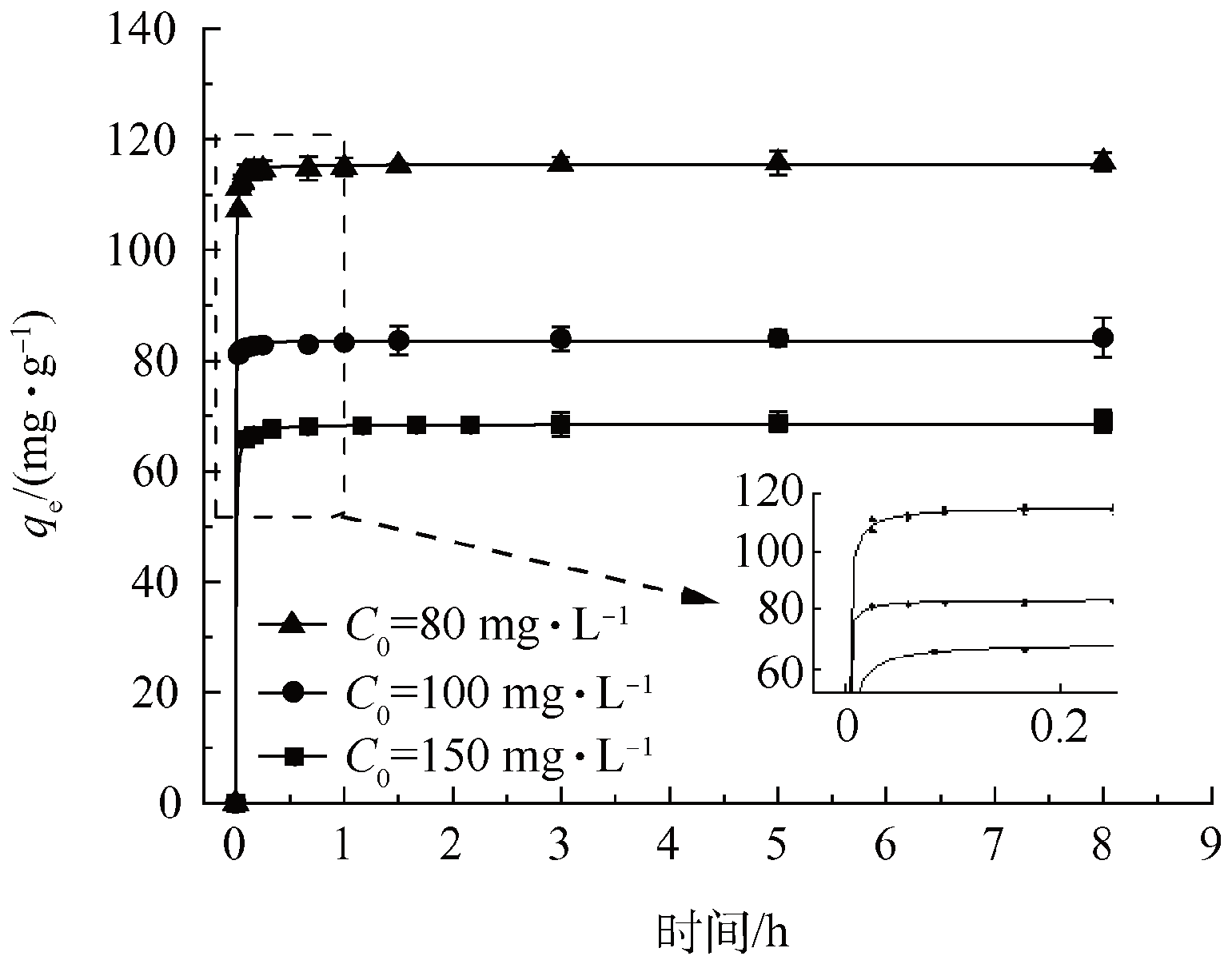
吸附动力学结果表明,LDHns-F3吸附磷酸盐在15 min左右达到平衡,并在8 h内达到完全平衡(图4)。实验结果采用伪二级动力学模型进行拟合,方程式表达如下:
t/qt = 1/k2qe2 + t/qe(3)
式中:qt为随时间变化的吸附量,mg・g−1;qe为平衡时的吸附量,mg・g−1;k2为反应速率常数,g・(mg・h)−1。拟合结果符合伪二级动力学模型(R2>0.999,表3),表明化学吸附可能是LDHns-F3吸附磷酸根的速率控制步骤。
表3 LDHns-F3吸附磷酸盐的伪二级动力学拟合参数
图4 LDHns-F3的吸附动力学实验及伪二级动力拟合
2.3 水滑石纳米片对磷酸盐的作用机理
2.3.1 Zeta电位分析
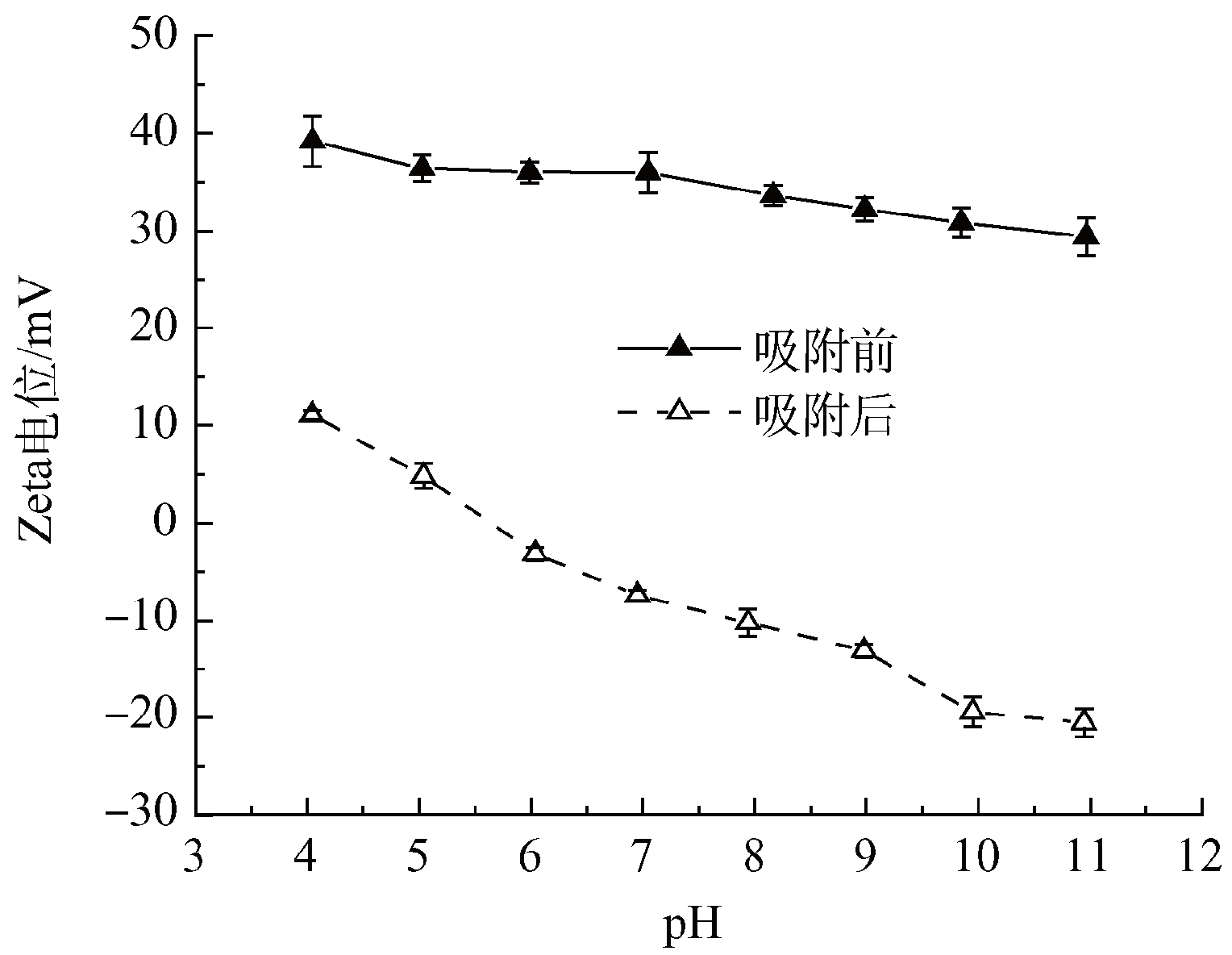
图5显示了LDHns-F3暴露在50 mg・L−1磷酸盐溶液前后的Zeta电位结果。吸附前,LDHns-F3的表面电荷全为正值,在pH范围4~11为29.4~39.2 mV。吸附后,LDHns-F3的表面电荷急剧下降,等电点为pH 5.7,之后的表面电荷全为负值,最低为-20.5 mV。表面电荷的减少表明,磷酸盐通过内层络合作用于吸附剂表面,因为外层络合物的形成不会改变材料的表面电荷。因此,Zeta电位测量有力地证明除了静电作用之外,磷酸盐还以共价结合的方式吸附在水滑石的层板上。
图5 LDHns-F3吸附前和吸附磷酸盐后的Zeta电位
2.3.2 X射线光电子能谱分析
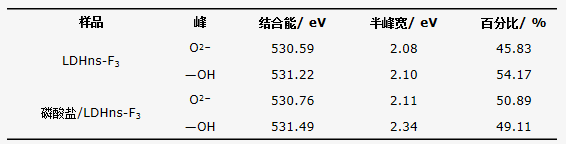
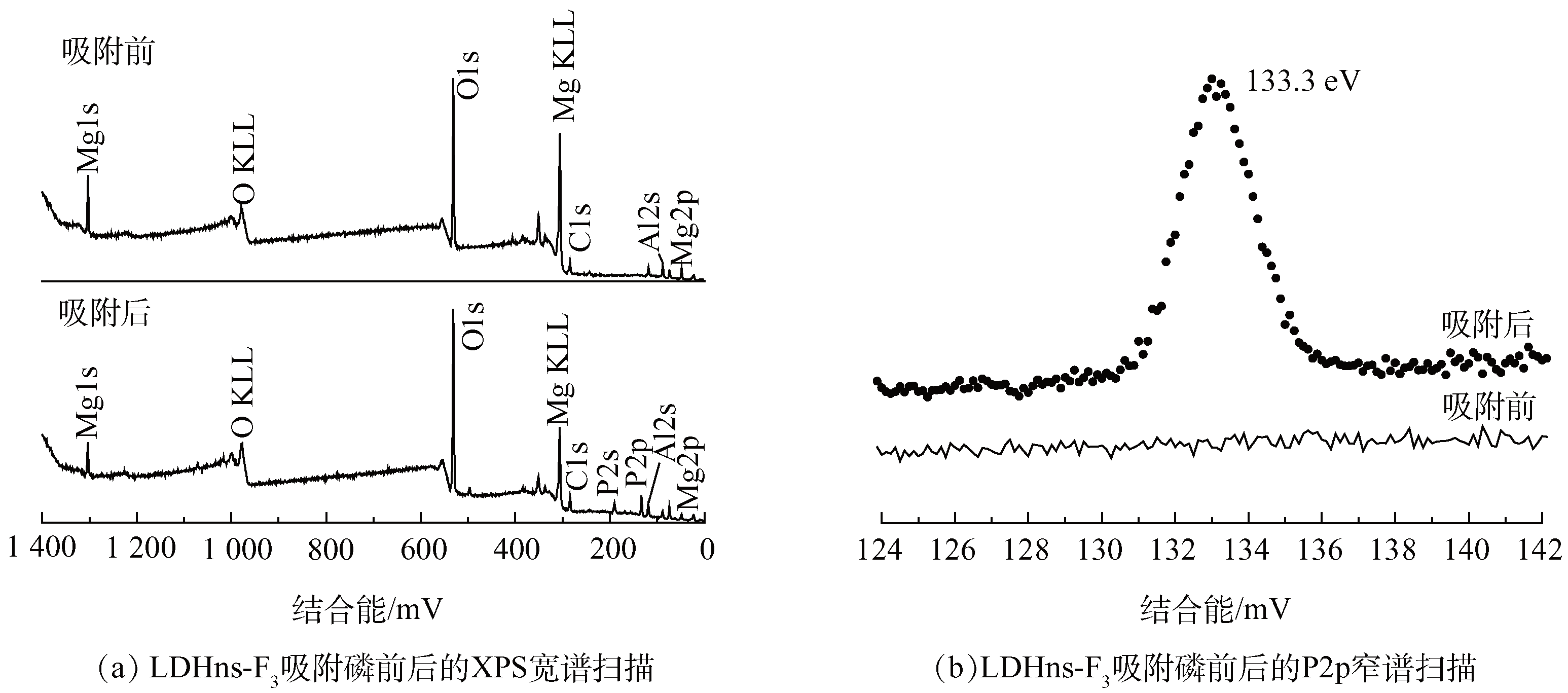
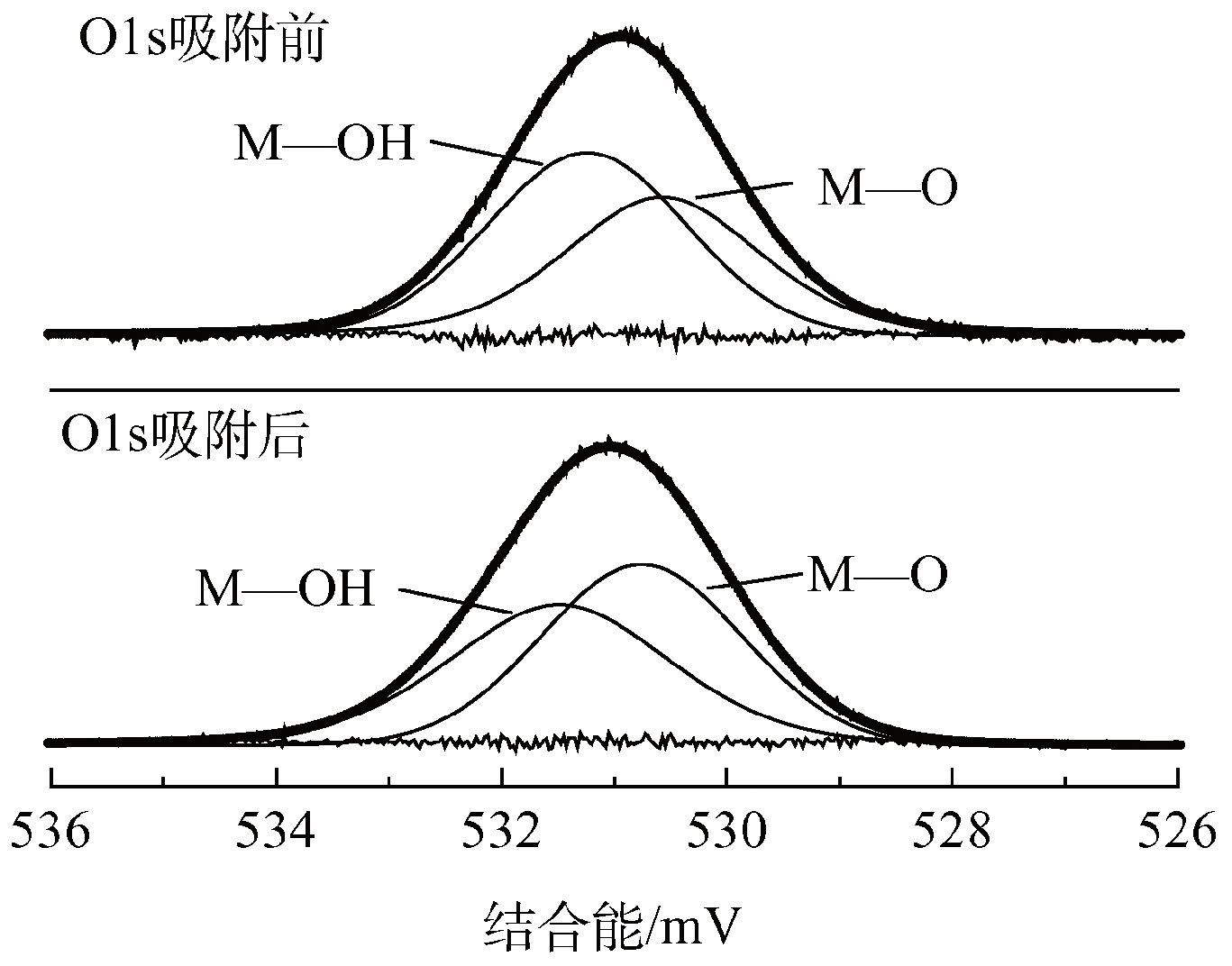
利用XPS进一步研究了吸附剂中官能团与磷酸根间的相互作用。XPS全谱扫描的LDHns-F3与吸附50 mg・L−1磷酸根后的光谱如图6(a)所示。吸附之后,在XPS宽谱和P2p窄谱(图6(b))中约133.3 eV处存在的峰表明,磷酸盐成功吸附到了水滑石纳米片上。根据不同形态的氧的结合能,对O1s的高分辨率扫描谱(图7)进行分峰,即M―O(氧与金属结合)和M―OH(羟基与金属结合)[34]。吸附前,LDHns-F3中M―O(530.59 eV)和M―OH(531.22 eV)的比例分别为45.83%和54.17%(表4)。吸附磷酸盐后,M―O的比例升高至50.89%,M―OH下降至49.11%。这一结果表明,水滑石纳米片吸附剂表面的羟基参与了磷酸盐的吸附过程。磷酸根可能通过形成M―O―P内层络合物结合到水滑石纳米片上,这与Zeta电位结果一致,同样表明层板上的羟基活性位在磷吸附中起到了重要作用。
表4 LDHns-F3的 XPS O1s谱中M―O和M―OH的分布
图6 LDHns-F3吸附磷前后的XPS图谱
图7 LDHns-F3吸附磷前后O1s的XPS图谱
2.4 水滑石纳米片的应用前景
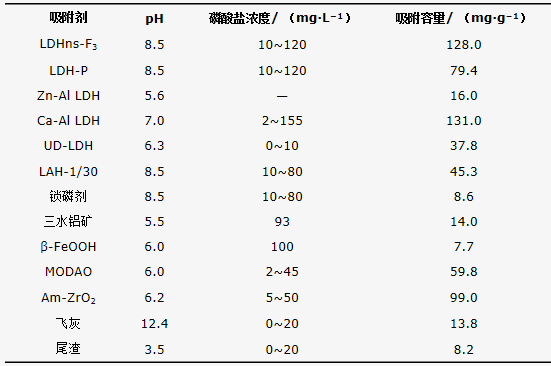
表5比较了多种吸附剂对磷酸盐的最大吸附容量。对比发现,本研究合成的LDHns-F纳米片的除磷能力高于其他大部分吸附剂,如Zn-Al LDH、三水铝矿、针铁矿、飞灰和锁磷剂Phoslock(镧改性膨润土,澳大利亚Phoslock Watar Solution Ltd.公司,已应用于世界上200多个富营养化湖泊磷污染控制)。水滑石纳米片吸附容量高于层状水滑石,机理在于纳米片的片层结构暴露出了更多的表面羟基吸附活性位点,而这些是在传统的LDHs中达不到的。表5显示,Ca-Al LDH的最大固磷量为131 mg・g−1,略高于本研究,但是这是吸附与表面沉淀共同作用的结果,含钙的水滑石比含镁的水滑石更容易溶解,溶解的钙会与磷形成磷酸钙沉淀反应。而且在pH低于8~9的情况下,沉淀会发生溶解,从而再次释放出磷酸盐。铁氧化物和氧化锆类吸附剂在天然水体或市政排水的pH条件下(6~9)通常带有负的表面电荷,因此,对于带负电荷的磷酸盐类污染物会形成一定的静电排斥作用,影响了材料的固磷效率。而本研究中的水滑石纳米片在pH 4~11的范围内,都能维持表面的正电荷,能够满足市政污水、工业废水和富营养化水体等多种含磷废水处理的使用需求。因此,LDH纳米片吸附效率高、容量大,且适用范围较广,是一种可用于处理高浓度含磷水体的高效吸附剂。
表5 不同吸附剂的最大吸附容量比较
3 结论
1)本研究利用甲酰胺一步合成法,在一定的镁铝反应物浓度范围内(Mg(NO3)2・6H2O不超过0.08 mol・L−1且 Al(NO3)3・9H2O不超过0.04 mol・L−1)合成了水滑石纳米片。但是当镁铝反应物的浓度增加到一定程度(Mg(NO3)2・6H2O达到0.10 mol・L−1且 Al(NO3)3・9H2O达到0.05 mol・L−1),纳米片会逐渐团聚。XRD结果显示,干燥后的水滑石纳米片具有层状水滑石特征峰,干燥过程在一定程度上造成了纳米片的堆叠。电镜结果显示水滑石纳米片具有超薄的特性,横向尺寸约30 nm,呈板状形貌和六角形微晶的特点。LDHns-F3的产量与已有研究相比提高了50倍,大大提高了吸附剂的合成效率并节约了成本。
2)合成的水滑石纳米片相比于传统方法合成的层状水滑石,展现出了优越的吸附能力。吸附等温线结果表明,使用Langmuir拟合LDHns-F3的饱和最大吸附量为128.0 mg・g−1,比层状水滑石LDH-P的吸附量提高了61%。吸附动力学结果表明,LDHns-F3能够迅速吸附磷酸盐并在15 min达到平衡,拟合结果符合伪二级动力学模型,表明化学吸附可能是LDHns-F3吸附磷酸根的速率控制步骤。
3)Zeta电位和XPS分析结果表明吸附的主要机制为磷酸盐在水滑石纳米片层板表面形成了内层络合物,吸附过程以化学吸附为主。(来源:环境工程学报 作者:刘晨)