ЦЋЖўМзыТ(UDMH)ЪЧвЛжжадФмСМКУЕФвКЬхЛ№М§ЭЦНјМСЁЃЫцзХКНЬьММЪѕЕФбИУЭЗЂеЙЃЌUDMHЪЙгУСПГжајдіЖрЃЌдкЪдбщЙ§ГЬжаЛсВњЩњДѓСПЕФгаЖОЗЯЫЎЁЃЯжНзЖЮЖдUDMHЗЯЫЎЕФДІРэЗНЗЈАќРЈЛЏбЇЁЂЮяРэЁЂЩњЮяЗНЗЈЕШЁЃГЃгУЛЏбЇЗНЗЈжївЊВЩгУбѕЛЏЙЄвеЃЌДцдкДІРэаЇТЪВЛИпЁЂФГаЉжаМфВњЮяЖОадДѓЁЂвзВњЩњЖўДЮЮлШОЕШШБЕуЁЃГЃгУЮяРэЗНЗЈжївЊВЩгУРызгНЛЛЛЪїжЌЁЂАМЭЙАєЭСЁЂЛюадЬПЕШЖдЗЯЫЎжаЮлШОЮяНјааЗжРыЁЂзЊвЦЃЌДцдкДІРэВЛГЙЕзЁЂЭЖзЪГЩБОНЯИпЁЂЮќИНМСдйЩњРЇФбЁЂЮќИНаЇЙћВЛМбЕШШБЕуЁЃГЃгУЩњЮяЗНЗЈВЩгУЯИОњЁЂЫЎЩњжВЮяЕШНЕНтUDMHЗЯЫЎЃЌДцдквзЪмНЕНтЛЗОГгАЯьЁЂНЕНтЫйТЪНЯТ§ЁЂдЫааПижЦНЯФбЕШЮЪЬтЁЃвЛаЉаТаЭЕФДІРэЙЄвеАќРЈГЌСйНчЫЎбѕЛЏЗЈЁЂЫсадбѕЛЏЕчЮЛЫЎДІРэММЪѕЁЂЕЭЮТЕШРызгЬхДІРэММЪѕЕШЁЃЦфжаГЌСйНчЫЎбѕЛЏЗЈПЩНЋФбНЕНтЕФДѓЗжзггаЛњЮядкЖЬЪБМфФкбѕЛЏЮЊNЃВЁЂHЃВOЁЂCOЃВЕШаЁЗжзгЮоЖОЮяжЪЃЌгУНсЙЙМђЕЅЧвЬхЛ§НЯаЁЕФЗДгІзАжУМДФмДяЕНбѕЛЏШЅГ§гаЛњЮяЕФФПЕФЃЌЕЋШБЕуЪЧДцдкЬѕМўМЋЦфбЯПСЃЌЧвЧАЦкЕФзАжУМлИёАКЙѓЃЌВЛФмзїЮЊГЃЙцНЕНтUD-MHЕФЙЄвеЃЛЫсадбѕЛЏЕчЮЛЫЎДІРэММЪѕЗДгІЫйЖШПьЃЌгШЦфБугкПьЫйДІРэНЯЕЭХЈЖШЁЂЩйСПЕФUDMHЗЯЫЎЃЌЕЋШдашгыЦфЫћЗЯЫЎДІРэММЪѕНсКЯЦ№РДЃЌвдзюДѓЯоЖШЬсИпUDMHЗЯЫЎДІРэаЇЙћЃЛЕЭЮТЕШРызгЬхДІРэММЪѕНЕНтНЯЮЊГЙЕзЁЂаЇЙћНЯМбЃЌЕЋЖдЩшБИвЊЧѓНЯИпЁЃвђДЫЃЌШчКЮЪЙгУИќЛЗБЃЧвАВШЋИпаЇЕФЙЄвеДІРэUDMHЗЯЫЎгазХМЋЦфживЊЕФвтвхЁЃ
дкЮЂВЈЗјЩфЯТЃЌЛюадЬПЮќЪеЮЂВЈФмСПВЂдкЦфБэУцаЮГЩКмЖрЁАШШЕуЁБЃЌИУЁАШШЕуЁБДІЕФФмСПМАЮТЖШБШЦфЫћЕиЗНИпГіаэЖрЃЌЭЈГЃБЛгУгкгеЕМЗДгІЕФДпЛЏМСЁЃФПЧАЃЌдкЛЗОГЙЄГЬСьгђЮЂВЈгеЕМДпЛЏММЪѕЭЦЙугІгУНЯЮЊЙуЗКЃЌдкФЃФтЕЅвЛГЩЗжЗЯЫЎНЕНтЗНУцВЩгУЮЂВЈ-ЛюадЬПЙЄвеЕФбаОПНЯЖрЁЃFen-tonЗЈдкИпХЈЖШЁЂФбНЕНтЗЯЫЎНЕНтСьгђгазХНЯЧПЕФгХЪЦЃЌвђЦфЩшБИМђвзЁЂЗбгУЩйЁЂВйзїМђЕЅЁЂЗДгІПьЫйЕШБЖЪмЧрэљЁЃ
дкЮЂВЈГЁжаЃЌFentonЪдМСДцдкЬѕМўЯТв§ШыЛюадЬПЃЌЛюадЬПЛюаджааФЩЯЮќИНFeЃВЃЋЁЂгаЛњЮлШОЮяЕШЃЌЖдєЧЛљздгЩЛљ(•OH)ИННќЮлШОЮяХЈЖШгадіДѓзїгУЃЌПЩЪЕЯжШЅГ§ЮлШОЮяЁЂдіЧПбѕЛЏаЇТЪЕФФПЕФЁЃЮЂВЈДЉЭИФмСІКмЧПЃЌгааЇНЕЕЭЗДгІЛюЛЏФмЃЌЖд•OHЪЭЗХгаРћЃЌдіДѓ•OHЩњГЩТЪЃЌЪЙFentonЗДгІЛюадДѓЗљЖШЬсИпЃЌФмШЁЕУНЯКУЕФНЕНтаЇЙћЁЃ
БОбаОПВЩгУЛюадЬП-ЮЂВЈ-FentonзщКЯММЪѕЖдUDMHЗЯЫЎНјааДІРэЃЌЬНЬжжївЊНЕНтжаМфВњЮяМзШЉгыЧшИљРызгЕФБфЛЏЙцТЩЃЌВЂЖдCODХЈЖШгыЪБМфЕФЙиЯЕНјааЯпадФтКЯЃЌвдЦкЮЊUDMHЗЯЫЎДІРэЕФЙЄвегІгУМАгХЛЏЬсЙЉРэТлВЮПМЁЃ
ЃБЁЂЪЕбщ
ЃБЃЎЃБ ЪдМСгывЧЦї
UDMHФЃФтЗЯЫЎЃЌгЩЦЋЖўМзыТбљЦЗгыШЅРызгЫЎХфжЦЖјГЩЃЌЦфжаUDMHжЪСПХЈЖШЮЊЃДЃАЃАmg/LЃЌCODжЪСПХЈЖШЮЊЃИЃВЃАmg/LЃЛЦЋЖўМзыТЃЌДПЖШЮЊЃЙЃЙЃЎЃВЃЅЃЌЮоЩЋЭИУїШмвКЃЛПХСЃЛюадЬПЃЌСЃОЖЃЗЃАЃА~ЃВЃГЃЖЃАІЬmЃЌЕтЮќИНжЕЃИЃЕЃАmg/gЃЌЧПЖШЃЙЃДЃЅЃЌЫЎЗжВЛДѓгкЃЕЃЅЃЌЛвЗжВЛДѓгкЃБЃЕЃЅЃЌБШБэУцЛ§ЃБЃВЃАЃАmЃВ/gЃЛжиИѕЫсМиЁЂЙ§бѕЛЏЧтЁЂСђЫсбЧЬњЁЂЧтбѕЛЏФЦЁЂСзЫсЧтЖўФЦЁЂМзДМЁЂАБЫЎЁЂАБЛљЛЧЫсяЇЁЂТШЛЏИЦЁЂСђЫсяЇЁЂСђЫсЁЂбЮЫсЁЂТШЛЏФЦЁЂФћУЪЫсЁЂввѕЃБћЭЊЁЂБљввЫсЁЂпСрЄ-АЭБШЭзЫсЁЂбЧЯѕЛљЬњЧшЛЏФЦЁЂввЫсяЇЃЌвдЩЯЪдМСОљЮЊЗжЮіДПЁЃ
ОИФзА(МгЛиСїРфФ§зАжУ)WPЃЗЃАЃА(MS-ЃВЃАЃАЃДTMS-ЃВЃАЃБЃДT)аЭLGЮЂВЈТЏЃЛPHS-ЃГCаЭЫсЖШМЦЃЛЃЗЃВЃБПЩМћЗжЙтЙтЖШМЦЫОЃЛDZF-ЃЖЃАЃВЃАецПеИЩдяЯфЃЛЃЗЃЙ-ЃБаЭДХСІНСАшЦїЃЛSHB-ЂѓбЛЗЫЎЪНЖргУецПеБУЁЃ
ЃБЃЎЃВ ЗжЮіВтЖЈЗНЗЈ
UDMHКЌСПВЩгУАБЛљбЧЬњЧшЛЏФЦЗжЙтЙтЖШЗЈВтЖЈЃЛCODКЌСПВЩгУЯћНтЗжЙтЙтЖШЗЈВтЖЈЃЛHCHOКЌСПВЩгУввѕЃБћЭЊЗЈНјааВтЖЈЃЛCNЃКЌСПВЩгУпСрЄ-АЭБШЭзЫсЗжЙтЙтЖШЗЈНјааВтЖЈЁЃ
ЃБЃЎЃГ ЪЕбщЗНЗЈ
ГЦШЁЪЪСППХСЃЛюадЬПЃЌгУжЪСПЗжЪ§ЮЊЃЕЃЅЕФЯЁбЮЫсНўХнЃВЃДhЃЌШЛКѓгУеєСѓЫЎЖрДЮСмЯДГЪжаадЃЌжУгкЃБЃГЃАЁцецПеИЩдяЯфИЩдяЃБЃВhжСКужиЃЌзАШыЯИПкЦПжаБИгУЁЃ
ЪвЮТЯТЃЌШЁвЛЖЈСПОДІРэКѓЕФЛюадЬПгкЃВЃЕЃАmLФЅПкЩеЦПжаЃЌМгШыЃБЃАЃАmLдЄЯШХфжЦКУЕФжЪСПХЈЖШЮЊЃДЃАЃАmg/LЕФUDMHЗЯЫЎЃЌЕїНкШмвКЕФpHжЕЃЌдйМгШыЪЪСПHЃВOЃВМАFeSOЃДШмвК(n(FeЃВЃЋ)ЁУn(HЃВOЃВ)АДЃБЁУЃЖЁЂЃБЁУЃИЁЂЃБЁУЃБЃАЁЂЃБЁУЃБЃВЗжБ№НјааХфжУ)ЁЃНЋЩеЦПжУгкЮЂВЈТЏЃЌДђПЊРфШДЫЎЃЌЕїНкЮЂВЈЙІТЪВЂЩшКУЪБМфПЊЪММгШШЁЃД§ЗДгІЭъШЋНсЪјКѓЃЌШЁГіЩеЦПВЂРфШДжСЪвЮТЃЌНЋЫЎбљЙ§ТЫЃЌВтЖЈдЪМЗЯЫЎМАДІРэКѓЕФЗЯЫЎдкЃЕЃАЃАnmДІЕФЮќЙтЖШжЕЃЌМЦЫуUDMHЕФШЅГ§ТЪЃЛВтЖЈCODжЕЃЌМЦЫуCODШЅГ§ТЪЃЛВтЖЈHCHOМАCNЃЕФКЌСПЁЃ
ЃВЁЂНсЙћгыЬжТл
ЃВЃЎЃБ HЃВOЃВЬхЛ§гыCODШЅГ§ТЪЕФЙиЯЕ
дкpHжЕЮЊЃГЁЂЮЂВЈЙІТЪЮЊЃДЃЖЃАWЁЂЛюадЬПжЪСПЮЊЃГgЁЂn(FeЃВЃЋ)ЁУn(HЃВOЃВ)ЃНЃБЁУЃБЃАЪБЃЌМгШыВЛЭЌЬхЛ§ЕФЃЖЃИЃЎЃЕg/LЕФHЃВOЃВШмвКЃЌвдЃЖЁЂЃБЃВЁЂЃБЃИЁЂЃВЃДЁЂЃГЃАminЮЊВЩбљЪБМфЕуЃЌHЃВOЃВЬхЛ§гыCODШЅГ§ТЪЕФЙиЯЕЧњЯпМћЭМЃБЁЃ
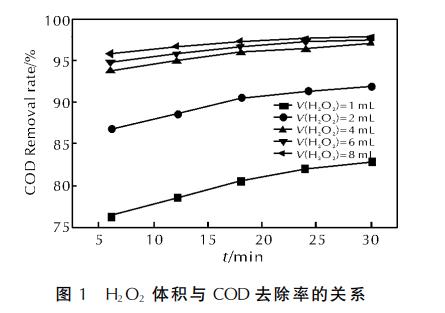
гЩЭМЃБПЩПДГіЃЌЫцзХHЃВOЃВЬхЛ§діЖрЃЌCODШЅГ§ТЪдіИпЁЃдкHЃВOЃВЬхЛ§ЮЊЃБmLЪБЃЌCODШЅГ§ТЪЯджјЕЭгкЃВЁЂЃДЁЂЃЖЁЂЃИmLЪБЕФжЕЁЃЕБЗДгІНјааЕНЃЖminЪБЃЌЬхЛ§ЮЊЃДЁЂЃЖЁЂЃИmLЕФCODШЅГ§ТЪМДПЩДяЃЙЃГЃЎЃЕЃЅвдЩЯЃЌЖјЕБЗДгІЪБМфбгГЄжСЃБЃА~ЃГЃАminЪБЃЌCODШЅГ§ТЪдіИпЗљЖШВЛДѓЁЃгЩДЫПЩЕУЃЌдкЮЂВЈЁЂЛюадЬПДцдкЯТЃЌFentonЗДгІдкНЯЖЬЕФЪБМфФкОЭФмЧїгкЦНКтЁЃЕБHЃВOЃВЬхЛ§діМгЕНЃДmLЪБЃЌCODдкЃГЃАminЪБЕФШЅГ§ТЪвбДяЃЙЃЗЃЎЃБЃЅЁЃетЪЧвђЮЊЃКЫцзХHЃВOЃВЬхЛ§ЕФдіМгЃЌ•OHЩњГЩЫйТЪдіМгЃЌЃВЃЋаЮГЩЫйТЪдіДѓЃЌЪЙЕУFeЃВЃЋЕФЩњГЩЫйТЪМгПьЃЌHЃВOЃВЗжНтЩњГЩ•OHЕФЫйТЪЫцжЎдіМгЁЃПМТЧЕНГЩБОвђЫиЃЌHЃВOЃВШЁЃДmLЮЊМбЁЃ
ЃВЃЎЃВ ЮЂВЈЙІТЪгыCODШЅГ§ТЪЕФЙиЯЕ
дкpHжЕЮЊЃГЁЂжЪСПХЈЖШЮЊЃЖЃИЃЎЃЕg/LЕФHЃВOЃВЬхЛ§ЮЊЃДЃЎЃАmLЁЂЛюадЬПжЪСПЮЊЃГgЁЂn(FeЃВЃЋ)ЁУn(HЃВOЃВ)ЃНЃБЁУЃБЃАЪБЃЌИФБфЮЂВЈЙІТЪЃЌвдЃЖЁЂЃБЃВЁЂЃБЃИЁЂЃВЃДЁЂЃГЃАminЮЊВЩбљЪБМфЕуЃЌЕУЕНЮЂВЈЙІТЪгыCODШЅГ§ТЪЕФЙиЯЕЧњЯпМћЭМЃВЁЃ
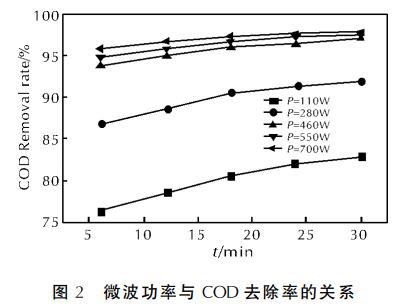
гЩЭМЃВПЩЕУЃЌЮЂВЈЙІТЪВЛЭЌЃЌCODШЅГ§ТЪОљЫцЪБМфбгГЄЖјдіИпЃЌЧвЙІТЪдНДѓЃЌШЅГ§ТЪОЭдНИпЃЌДяЕНЦНКтЫљашЪБМфОЭдНЖЬЁЃЕБНјааЕНЃГЃАminЪБЃЌЃДЃЖЃАЁЂЃЕЃЕЃАЁЂЃЗЃАЃАWЬѕМўЯТЕФCODШЅГ§ТЪЖМЧїгкЃЙЃЗЃЅ~ЃЙЃИЃЅЁЃдіДѓЮЂВЈЙІТЪЃЌЫфФмдіМгFentonЗДгІЫйТЪЃЌЕЋЖдCODШЅГ§ТЪгАЯьЩѕЮЂЁЃЗжЮіШЯЮЊЃЌдіДѓЮЂВЈЙІТЪЃЌЪЙFentonЗДгІЫйТЪЬсИпЃЛЭЌЪБЃЌПЩЪЙЛюадЬПБэУцЕФЁАШШЕуЁБЪ§СПдіМгЃЌЧПЛЏЛюадЬПЖдCODЕФЮќИНзїгУЃЌЪЙЕУШЅГ§ТЪдіИпЁЃзлКЯПМТЧЃЌЮЂВЈЙІТЪбЁШЁЃДЃЖЃАWзюМбЁЃ
ЃВЃЎЃГ pHжЕгыCODШЅГ§ТЪЕФЙиЯЕ
дкЮЂВЈЙІТЪЮЊЃДЃЖЃАWЁЂЃЖЃИЃЎЃЕg/LЕФHЃВOЃВЬхЛ§ЮЊЃДЃЎЃАmLЁЂЛюадЬПжЪСПЮЊЃГgЁЂn(FeЃВЃЋ)ЁУn(HЃВOЃВ)ЃНЃБЁУЃБЃАЪБЃЌИФБфpHжЕЃЌПМВьЦфЖдCODШЅГ§ТЪЕФгАЯьЃЌНсЙћМћЭМЃГЁЃ
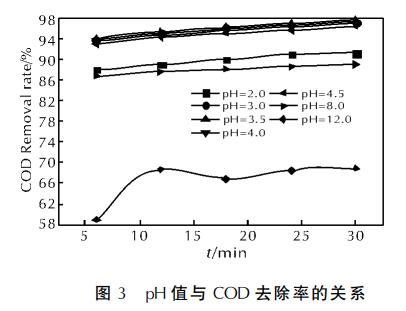
ДгЭМЃГПЩПДГіЃЌCODдкЗДгІЧАЃЖminФкШЅГ§НЯЮЊУїЯдЁЃЕБpHжЕЗжБ№ЮЊЃВЁЂЃГЁЂЃГЃЎЃЕЁЂЃДЁЂЃДЃЎЃЕЁЂЃИЪБЃЌЗДгІдкЃЖminФкCODШЅГ§ТЪвбНЯДѓЃЌЖјКѓЧїгкЦНКтЁЃpHжЕЮЊЃГЃЎЃЕЪБCODШЅГ§ТЪзюИпЃЌДяЃЙЃЗЃЎЃЕЃЅЁЃЖјЕБpHжЕЮЊЃБЃВГЪШѕМюадЪБЃЌCODШЅГ§ТЪНіЮЊЃЖЃИЃЎЃЙЃЅЁЃ
дкpHжЕДѓгкЃЗЪБЃЌHЃЋШнвзКЭOHЃЯрНсКЯЃЌГ§СЫгаРћгк•OHЩњГЩЭтЃЌЛЙДйНјЛюадЬПЖдCODЕФЮќИНЁЃpHжЕдіИпЃЌЖд•OHЕФЪЭЗХгавжжЦзїгУЁЃЕЋpHжЕЙ§ЕЭЃЌHЃЋвжжЦFeЃГЃЋГЏFeЃВЃЋзЊЛЏЃЌМДFeЃГЃЋВЛФмБЛЛЙдЮЊFeЃВЃЋЁЃЕБpHжЕЙ§ИпЪБЃЌFeЃГЃЋКЭOHЃвзгкЩњГЩFe(OH)ЃГГСЕэЃЌвжжЦFentonЗДгІЕФНјааЁЃpHЃНЃИЕФШѕМюадЛЗОГЯТЃЌCODШЅГ§ТЪПЩДяЃИЃЙЃЅЃЌетЫЕУїЮЂВЈЁЂЛюадЬПЕФДцдкПЩдквЛЖЈГЬЖШЩЯЯїШѕpHжЕЖдFentonЗДгІЫљдьГЩЕФИКУцгАЯьЁЃБОЪЕбщЬѕМўЯТЃЌpHжЕбЁЃГЃЎЃЕНЯЮЊЪЪвЫЃЌетгыFentonЪдМСЕФpHжЕЪЙгУЗЖЮЇвЛжТЁЃ
ЃВЃЎЃД FeЃВЃЋЭЖШыСПгыCODШЅГ§ТЪЕФЙиЯЕ
дкpHжЕЮЊЃГЃЎЃЕЁЂЮЂВЈЙІТЪЮЊЃДЃЖЃАWЁЂЃЖЃИЃЎЃЕg/LЕФHЃВOЃВЬхЛ§ЮЊЃДЃЎЃАmLЁЂЛюадЬПжЪСПЮЊЃГgЪБЃЌвдn(FeЃВЃЋ)ЁУn(HЃВOЃВ)ЗжБ№ЮЊЃБЁУЃЖЁЂЃБЁУЃИЁЂЃБЁУЃБЃАЁЂЃБЁУЃБЃВЖдUDMHЗЯЫЎНјааДІРэЃЌЪЕбщНсЙћМћЭМЃДЁЃ
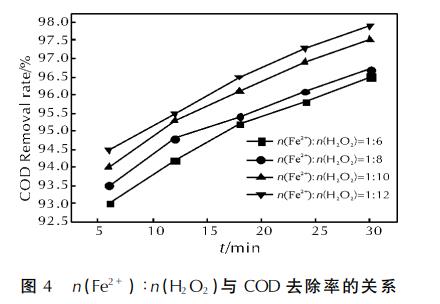
гЩЭМЃДПЩПДГіЃЌЫцзХn(FeЃВЃЋ)ЁУn(HЃВOЃВ)ЕФМѕаЁЃЌCODШЅГ§ТЪдіИпЃЌЕЋИїn(FeЃВЃЋ)ЁУn(HЃВOЃВ)БШжЕЬѕМўЯТЕФCODШЅГ§ТЪдіЗљВЛЬЋУїЯдЃЌБШжЕЮЊЃБЁУЃЖгыЃБЁУЃИЪБЕФCODШЅГ§ТЪНЯЮЊНгНќЃЌЗДгІЃГЃАminЪБПЩДяЃЙЃЖЃЎЃЕЃЅвдЩЯЃЛБШжЕЮЊЃБЁУЃБЃАгыЃБЁУЃБЃВЪБЕФCODШЅГ§ТЪЯрВюВЛДѓЃЌЗДгІЃГЃАminЪБПЩДяЃЙЃЗЃЎЃЕЃЅвдЩЯЁЃетЫЕУїFeЃВЃЋЪЧДйЪЙHЃВOЃВЗжНтВњЩњ•OHЕФДпЛЏМСЁЃFeЃВЃЋХЈЖШВЛИпЪБЃЌHЃВOЃВНЯФбВњЩњ•OHЃЌЗДгІЫйТЪЕЭЃЛЫцзХFeЃВЃЋХЈЖШЕФдіДѓЃЌЗДгІЫйТЪМгПьЃЛFeЃВЃЋХЈЖШМЬајдіМгЃЌЙ§СПFeЃВЃЋПЩФмКЭ•OHЦ№ЗДгІЃЌВЛЖЯЯћКФЕє•OHЃЌЪЙFentonЗДгІЫйТЪМѕТ§ЃЌНЕЕЭCODШЅГ§ТЪЁЃвђДЫЃЌбЁдёn(FeЃВЃЋ)ЁУn(HЃВOЃВ)ЃНЃБЁУЃБЃАНЯЮЊКЯЪЪЁЃ
ЃВЃЎЃЕ ЛюадЬПЭЖШыСПгыCODШЅГ§ТЪЕФЙиЯЕ
дкpHжЕЮЊЃГЃЎЃЕЁЂЮЂВЈЙІТЪЮЊЃДЃЖЃАWЁЂЃЖЃИЃЎЃЕg/LЕФHЃВOЃВЬхЛ§ЮЊЃДЃЎЃАmLЁЂn(FeЃВЃЋ)ЁУn(HЃВOЃВ)ЃНЃБЁУЃБЃАЪБЃЌЕїећЛюадЬПгУСПЃЌПМВьЦфЖдДІРэаЇЙћЕФгАЯьГЬЖШЃЌНсЙћМћЭМЃЕЁЃ
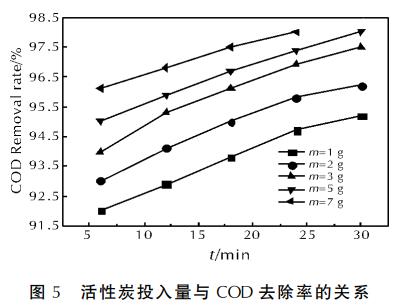
гЩЭМЃЕПЩПДГіЃЌЫцзХЛюадЬПЭЖШыСПЕФдіДѓЃЌCODШЅГ§ТЪдіИпЁЃетЪЧгЩгкЛюадЬПгазХСМКУЕФЮќИНзїгУЃЌЛюадЬПгУСПдНЖрЃЌБШБэУцЛ§дНДѓЃЌЮќИНадФмдНКУЁЃЫцзХЛюадЬПЭЖШыСПЕФдіМгЃЌдНРДдНЖрЕФЁАШШЕуЁБ(дкЮЂВЈЗјЩфЯТЃЌПЩЙлВьЕНЛюадЬПБэУцГіЯжЛ№ЛЈ)дкЮЂВЈГЁжааЮГЩЃЌДЫЁАШШЕуЁБДІФмСПгыЮТЖШБШЦфЫћЕиЗНИпГіаэЖрЃЌБЛЮќИНЕФЮяжЪвзгкдкИУЮЛЕуЩЯЗЂЩњЮяРэЛЏбЇзїгУЃЌДпЛЏНЕНтЫйТЪМгПьЃЌЖдЮлШОЮяЕФШЅГ§гаРћЁЃетжжНЋЮЂВЈФмСПЕУвдОлМЏВЂЪЭЗХИјЫЎжаЮлШОЮяЪЙжЎбѕЛЏЗжНтЕФНсЙћБэУїЃЌЛюадЬПЕФзїгУЗћКЯДпЛЏМСЕФЖЈвхЃЌдкБОЗДгІжаЛюадЬПМИКѕЮоЯћКФЁЃCODШЅГ§ТЪдкЛюадЬПжЪСПЮЊЃЗgЪБДязюИпЁЃЕЋЕБЛюадЬПжЪСПДѓгкЃЕgКѓЃЌCODШЅГ§ТЪНіТдЮЊдіИпЁЃвђДЫЃЌбЁШЁЃЕgЛюадЬПНјааЪЕбщбаОПЁЃ
ЃВЃЎЃЖ зюМбЪЕбщЬѕМўЯТUDMHЕФНЕНт
дкЮЂВЈЙІТЪЮЊЃДЃЖЃАWЁЂЃЖЃИЃЎЃЕg/LЕФHЃВOЃВЬхЛ§ЮЊЃДmLЁЂpHжЕЮЊЃГЃЎЃЕЁЂn(FeЃВЃЋ)ЁУn(HЃВOЃВ)ЃНЃБЁУЃБЃАЁЂЛюадЬПжЪСПЮЊЃЕgЕФЬѕМўЯТЃЌвдЃЖЁЂЃБЃВЁЂЃБЃИЁЂЃВЃДЁЂЃГЃАminЮЊВЩбљЪБМфЕуЃЌЗЯЫЎUDMHЕФШЅГ§ТЪЗжБ№ЮЊЃЙЃЖЃЅЁЂЃЙЃЗЃЎЃБЃЅЁЂЃЙЃЗЃЎЃЙЃЅЁЂЃЙЃИЃЎЃИЃЅЁЂЃЙЃЙЃЎЃГЃЅЁЃПЩвдПДГіЃЌЛюадЬП-ЮЂВЈ-FentonЬхЯЕдкЪЕбщНјааЕНЃГЃАminЪБЃЌUDMHШЅГ§ТЪИпДяЃЙЃЙЃЎЃГЃЅЁЃЮЂВЈЗјЩфПЩМгПьЛюадЬПЮќИНДпЛЏНЕНтUDMHЫйТЪЃЌЖдЮќИНЬхЛ§Ц№діДѓзїгУЁЃдкЮЂВЈГЁжаЃЌHЃВOЃВвзЪЭЗХ•OHЃЌЪЙЗДгІЛюЛЏФмНЕЕЭЃЌМгЫйFentonЕФЗДгІНјГЬЁЃHЃВOЃВЁЂFeЃВЃЋЁЂЮЂВЈЁЂЛюадЬПЕФаЭЌаЇгІЯджјЬсИпСЫЬхЯЕЕФбѕЛЏФмСІЃЌЪЙЕУЗЯЫЎжаUDMHМАCODОљгаКмИпЕФШЅГ§ТЪЁЃ
ЃВЃЎЃЗ НЕНтЙ§ГЬжажївЊжаМфВњЮяЕФБфЛЏЙцТЩ
UDMHНЕНтЙ§ГЬжажаМфВњЮяжївЊЮЊМзШЉЁЂЧшИљРызгЃЌКЌСПНЯИпЁЂЖОадНЯДѓЃЌЧвДцдкЪБМфНЯГЄЁЃ
ЃВЃЎЃЗЃЎЃБ МзШЉЕФБфЛЏЙцТЩ
дкЮЂВЈЙІТЪЮЊЃДЃЖЃАWЁЂЃЖЃИЃЎЃЕg/LЕФHЃВOЃВЬхЛ§ЮЊЃДmLЁЂpHжЕЮЊЃГЃЎЃЕЁЂn(FeЃВЃЋ)ЁУn(HЃВOЃВ)ЃНЃБЁУЃБЃАЁЂЛюадЬПжЪСПЮЊЃЕgЕФЬѕМўЯТЃЌЗжЮіЗЯЫЎжаМзШЉЕФжЪСПХЈЖШЫцЪБМфЕФБфЛЏЙцТЩЃЌНсЙћШчЭМЃЖЫљЪОЁЃ
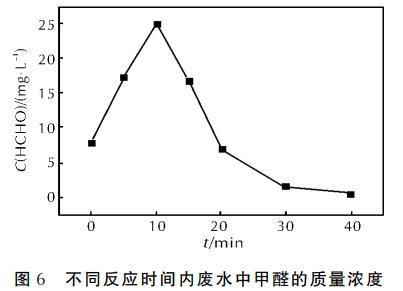
гЩЭМЃЖПЩжЊЃЌЮДОДІРэЕФЗЯЫЎжавбКЌгажЪСПХЈЖШЮЊЃЗЃЎЃЙmg/LЕФМзШЉЃЌетПЩФмЪЧгЩгкОУжУЕФдЕЙЪЃЌгаЩйСПМзШЉЩњГЩЁЃЫцзХЗДгІЪБМфЕФбгГЄЃЌUDMHж№НЅНЕНтЃЌМзШЉЕФжЪСПХЈЖШЗЂЩњСЫБфЛЏЁЃЗДгІЦ№ЪМЃЌМзШЉЕФжЪСПХЈЖШМБОчдіМгЃЌЃБЃАminЪБДяЕНЗхжЕЁЃДЫКѓЃЌМзШЉжЪСПХЈЖШбИЫйНЕЕЭЃЌдкЃГЃАminДІМзШЉжЪСПХЈЖШвбОМЋЩйЃЌетБэУїМзШЉЪЧЛюадЬП-ЮЂВЈ-FentonЗДгІНЕНтUDMHЕФвЛжжжаМфВњЮяЁЃДЫЭтЃЌМзШЉжЪСПХЈЖШдкЃБЃАminКѓГЪжБЯпзДНЕЕЭвВжЄУїСЫИУЗДгІЬхЯЕОпгаГЌЧПЕФбѕЛЏФмСІЁЃ
ЃВЃЎЃЗЃЎЃВ ЧшИљРызгЕФБфЛЏЙцТЩ
дкЮЂВЈЙІТЪЮЊЃДЃЖЃАWЁЂЃЖЃИЃЎЃЕg/LЕФHЃВOЃВЬхЛ§ЮЊЃДmLЁЂpHжЕЮЊЃГЃЎЃЕЁЂn(FeЃВЃЋ)ЁУn(HЃВOЃВ)ЃНЃБЁУЃБЃАЁЂЛюадЬПжЪСПЮЊЃЕgЕФЬѕМўЯТЃЌЗжЮіЗЯЫЎжаЧшИљРызг(CNЃ)ЕФжЪСПХЈЖШЫцЪБМфЕФБфЛЏЃЌНсЙћШчЭМЃЗЫљЪОЁЃ
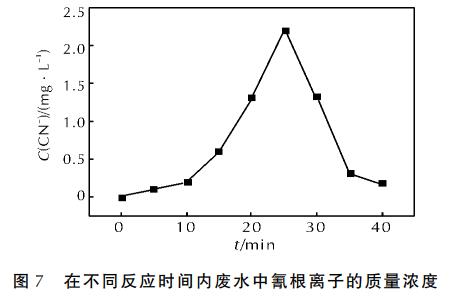
ДгЭМЃЗПЩвдПДГіЃЌЮДОДІРэЕФЗЯЫЎжаЪЧВЛКЌCNЃЕФЁЃЫцзХЗДгІЪБМфЕФбгГЄЃЌCNЃОРњСЫДгЩњГЩжСДяЕНжЪСПХЈЖШзюИпжЕЃЌШЛКѓбИЫйНЕЕЭЕФЙ§ГЬЁЃдкЗДгІПЊЪМЪБЃЌЫцзХUDMHЕФНЕНтЃЌCNЃвВЫцжЎВњЩњЃЌЃВЃЕminЪБжЪСПХЈЖШДяЕНзюДѓжЕЁЃжЎКѓCNЃбИЫйБЛбѕЛЏЃЌдкЃДЃАminДІCNЃЛљБОЯћГ§ЁЃгЩДЫПЩжЊЃЌЫфШЛCNЃЪЧвЛжжНЯФбНЕНтЕФжаМфВњЮяЃЌЕЋдкЛюадЬП-ЮЂВЈ-FentonЗДгІЬхЯЕжаЛљБОПЩвдНЕНтЭъШЋЁЃетЫЕУїИУЗДгІЬхЯЕВЛНіЖдUDMHЁЂCODгаКмКУЕФШЅГ§аЇЙћЃЌЖдUDMHЕФжаМфВњЮяМзШЉЁЂЧшИљРызгЭЌбљПЩДяЕНКмКУЕФНЕНтаЇЙћЁЃ
ЃВЃЎЃИ ЗДгІЖЏСІбЇЗНГЬ
гЩЩЯЪізюМбЗДгІЬхЯЕДІРэЗЯЫЎЕФНсЙћЃЌЬНЬжCODШЅГ§ТЪЕФЖЏСІбЇЙцТЩЁЃвдЗДгІЪБМфtЮЊКсзјБъЁЂln(CЃА/C)ЮЊзнзјБъзїЭМ(CЃАЮЊЗЯЫЎЫЎбљжаCODЕФГѕЪМжЪСПХЈЖШЃЌCЮЊДІРэКѓЫЎбљжаCODЕФжЪСПХЈЖШ)ЃЌНсЙћШчЭМЃИЫљЪОЁЃ
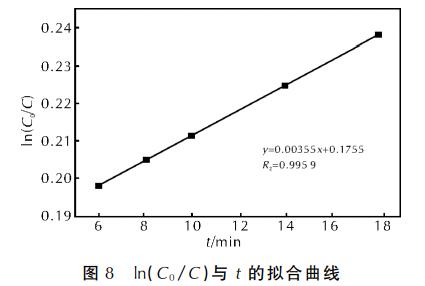
гЩЭМЃИПЩЕУЃЌЗЯЫЎжаЕФCODШЅГ§ТЪзёбвЛМЖЗДгІЖЏСІбЇЬиеїЃЌЖЏСІбЇЗНГЬЮЊЃКln(CЃА/C)ЃНЃАЃЎЃАЃАЃГЃЕЃЕtЃЋЃАЃЎЃБЃЗЃЕЃЕЃЌRЃВЃНЃАЃЎЃЙЃЙЃЕЃЙЃЌБэУїИУФтКЯНсЙћНЯЮЊРэЯыЁЃ
ЃГЁЂНсТл
(ЃБ)ЭЈЙ§ЛюадЬП-ЮЂВЈ-FentonСЊгУММЪѕЖдUDMHЗЯЫЎНјааДІРэЃЌЕУЕНЕФзюМбЗДгІЬѕМўЮЊЃКЮЂВЈЙІТЪЮЊЃДЃЖЃАWЁЂЃЖЃИЃЎЃЕg/LЕФHЃВOЃВЬхЛ§ЮЊЃДmLЁЂpHжЕЮЊЃГЃЎЃЕЁЂn(FeЃВЃЋ)ЁУn(HЃВOЃВ)ЃНЃБЁУЃБЃАЁЂЛюадЬПжЪСПЮЊЃЕgЁЂЗДгІЪБМфЮЊЃГЃАminЃЛдкзюМбЗДгІЬѕМўЯТЃЌГѕЪМжЪСПХЈЖШЮЊЃДЃАЃАmg/LЕФUDMHЗЯЫЎШЅГ§ТЪЮЊЃЙЃЙЃЎЃГЃЅЃЌCODШЅГ§ТЪПЩДяЃЙЃИЃЎЃАЃЅЁЃДЫЭтЃЌЛЙПЩгааЇНЕНтМзШЉМАЧшИљРызгЕШжаМфВњЮяЁЃ
(ЃВ)ЗДгІЖЏСІбЇбаОПБэУїЃЌЗЯЫЎжаЕФCODШЅГ§ТЪзёбвЛМЖЗДгІЖЏСІбЇЬиеїЃЌЖЏСІбЇЗНГЬЮЊЃКln(CЃА/C)ЃНЃАЃЎЃАЃАЃГЃЕЃЕtЃЋЃАЃЎЃБЃЗЃЕЃЕЃЌЯрЙиадДяЃАЃЎЃЙЃЙЃЕЃЙЁЃ
(ЃГ)ЛюадЬП-ЮЂВЈ-FentonзщКЯММЪѕДІРэUDMHЗЯЫЎЃЌдкЗДгІПЊЪМЃЖminФкМДПЩДяЕННЯЮЊРэЯыЕФаЇЙћЃЌОпгаЗДгІбИЫйЕФЬиЕуЁЃДЫЭтЃЌИУММЪѕВйзїЗНБуЁЂГЩБОЕЭСЎЁЂЮоЖўДЮЮлШОЁЂзАжУМђЕЅЧвеМЕиУцЛ§аЁЁЂгаЛњЮяПѓЛЏЖШИпЃЌЪЧвЛжжИпаЇЕФUDMHЗЯЫЎДІРэММЪѕЁЃЃЈРДдДЃКЩЯКЃПеМфЭЦНјбаОПЫљЃЌЩЯКЃПеМфЗЂЖЏЛњЙЄГЬММЪѕбаОПжааФЃЉ



